Коррозия — это самопроизвольно протекающий процесс разрушения металлов в результате химического или электрохимического взаимодействия их с окружающей средой.
Электрохимическая коррозия — наиболее распространенный вид коррозии металлов, это разрушение металла в среде электролита с возникновением внутри системы электрического тока. Примером коррозионных процессов электрохимического характера является разрушение деталей машин и различных металлических конструкций в почвенных, грунтовых, речных и морских водах, во влажной атмосфере, в технических растворах, под действием смазочно-охлаждающих жидкостей, применяемых при механической обработке металлов и т.д.
Причиной электрохимической коррозии является образование на поверхности металла большого количества микрогальванических пар, которые возникают по следующим причинам:
1. Наличие примесей металлов или других веществ, отличающихся по активности от основного металла.
2. Структурная неоднородность поверхности металла, что определяет наличие участков с разной активностью.
3. Неравномерность распределения деформаций в металле после термической и механической обработки и др.
При электрохимической коррозии на поверхности металла одновременно протекают два процесса:
— анодный — окисление металла: Ме — n? = Men+
— катодный — восстановление ионов водорода в кислой среде:
2H+ + 2e = H2 или молекул кислорода, растворенного в воде, в случае атмосферной коррозии:
2H2O + O2 + 4? = 4OH-.
Ионы или молекулы, которые восстанавливаются на катоде, называются деполяризаторами. При атмосферной коррозии — коррозии во влажном воздухе при комнатной температуре — деполяризатором является кислород.
Пример 20. Как происходит коррозия цинка, находящегося в контакте с кадмием в нейтральном и кислом растворах? Составьте электронные уравнения анодного и катодного процессов. Каков состав продуктов коррозии?
Решение. При таком контакте возникает коррозионный гальванический микроэлемент. Цинк имеет более отрицательный потенциал (-0,763 В), чем кадмий (-0,403) (табл. 12.1), поэтому он является анодом, а кадмий — катодом.
Анодный процесс: Zn — 2? = Zn2+ .
Катодный процесс: в кислой среде: 2H+ + 2? = H2 ;
в нейтральной среде: 2H2O + O2 + 4? = 4OH- .
Так как ионы Zn2+ с гидроксильной группой образуют нерастворимый гидроксид, то продуктом коррозии в нейтральной среде будет Zn(OH)2.
Скорость коррозии тем больше, чем сильнее различаются электродные потенциалы металлов, т.е. чем дальше они расположены друг от друга в ряду напряжений. Кроме того, скорость коррозии повышается при увеличении концентрации электролита и повышении температуры.
Определение коррозии
Материалы из металлов под химическим или электрохимическим воздействием окружающей среды подвергаются разрушению, которое называется коррозией.
Коррозия металлов вызывается окислительно-восстановительными реакциями, в результате которых металлы переходят в окисленную форму и теряют свои свойства, что приводит в негодность металлические материалы.
Можно выделить 3 признака, характеризующих коррозию:
- Коррозия – это с химической точки зрения процесс окислительно-восстановительный.
- Коррозия – это самопроизвольный процесс, возникающий по причине неустойчивости термодинамической системы металл – компоненты окружающей среды.
- Коррозия – это процесс, который развивается в основном на поверхности металла. Однако, не исключено, что коррозия может проникнуть и вглубь металла.
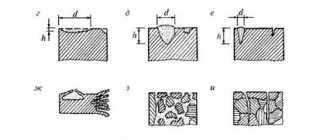
Виды коррозии металлов
Наиболее часто встречаются следующие виды коррозии металлов:
- Равномерная – охватывает всю поверхность равномерно
- Неравномерная
- Избирательная
- Местная пятнами – корродируют отдельные участки поверхности
- Язвенная (или питтинг)
- Точечная
- Межкристаллитная – распространяется вдоль границ кристалла металла
- Растрескивающая
- Подповерхностная
Основные виды коррозии металлов
С точки зрения механизма коррозионного процесса можно выделить два основных типа коррозии: химическую и электрохимическую.
Электрохимическая коррозия металлов
Электрохимическая коррозия металлов – это процесс разрушения металлов в среде различных электролитов, который сопровождается возникновением внутри системы электрического тока.
При таком типе коррозии атом удаляется из кристаллической решетки результате двух сопряженных процессов:
- Анодного – металл в виде ионов переходит в раствор.
- Катодного – образовавшиеся при анодном процессе электроны, связываются деполяризатором (вещество — окислитель).
Сам процесс отвода электронов с катодных участков называется деполяризацией, а вещества способствующие отводу – деполяризаторами.
Наибольшее распространение имеет коррозия металлов с водородной и кислородной деполяризацией.
Водородная деполяризация
Водородная деполяризация осуществляется на катоде при электрохимической коррозии в кислой среде:
2H++2e— = H2 разряд водородных ионов
2H3O++2e— = H2 + 2H2O
Кислородная деполяризация
Кислородная деполяризация осуществляется на катоде при электрохимической коррозии в нейтральной среде:
O2 + 4H++4e— = H2O восстановление растворенного кислорода
O2 + 2H2O + 4e— = 4OH—
Все металлы, по их отношению к электрохимической коррозии, можно разбить на 4 группы, которые определяются величинами их стандартных электродных потенциалов:
- Активные металлы (высокая термодинамическая нестабильность) – это все металлы, находящиеся в интервале щелочные металлы — кадмий (Е0 = -0,4 В). Их коррозия возможна даже в нейтральных водных средах, в которых отсутствуют кислород или другие окислители.
- Металлы средней активности (термодинамическая нестабильность) – располагаются между кадмием и водородом (Е0 = 0,0 В). В нейтральных средах, в отсутствии кислорода, не корродируют, но подвергаются коррозии в кислых средах.
- Малоактивные металлы (промежуточная термодинамическая стабильность) – находятся между водородом и родием (Е0 = +0,8 В). Они устойчивы к коррозии в нейтральных и кислых средах, в которых отсутствует кислород или другие окислители.
- Благородные металлы (высокая термодинамическая стабильность) – золото, платина, иридий, палладий. Могут подвергаться коррозии лишь в кислых средах при наличии в них сильных окислителей.
Виды электрохимической коррозии
Электрохимическая коррозия может протекать в различных средах. В зависимости от характера среды выделяют следующие виды электрохимической коррозии:
- Коррозия в растворах электролитов — в растворах кислот, оснований, солей, в природной воде.
- Атмосферная коррозия – в атмосферных условиях и в среде любого влажного газа. Это самый распространенный вид коррозии.
Например, при взаимодействии железа с компонентами окружающей среды, некоторые его участки служат анодом, где происходит окисление железа, а другие – катодом, где происходит восстановление кислорода:
А: Fe – 2e— = Fe2+
K: O2 + 4H+ + 4e— = 2H2O
Катодом является та поверхность, где больше приток кислорода.
- Почвенная коррозия – в зависимости от состава почв, а также ее аэрации, коррозия может протекать более или менее интенсивно. Кислые почвы наиболее агрессивны, а песчаные – наименее.
- Аэрационная коррозия — возникает при неравномерном доступе воздуха к различным частям материала.
- Морская коррозия – протекает в морской воде, в связи с наличием в ней растворенных солей, газов и органических веществ.
- Биокоррозия – возникает в результате жизнедеятельности бактерий и других организмов, вырабатывающих такие газы как CO2, H2S и др., способствующие коррозии металла.
- Электрокоррозия – происходит под действием блуждающих токов на подземных сооружениях, в результате работ электрических железных дорог, трамвайных линий и других агрегатов.
Коррозия блуждающими токами (электрокоррозия) и защита
Атмосферная коррозия
Атмосферная коррозия – это коррозия металлов в условиях земной атмосферы (во влажном воздухе и температуре окружающей среды). Она наиболее распространена. Имеет ряд специфических ее особенностей. Коррозионной средой (электролитом) является вода, в которой присутствуют кислород воздуха (окислитель), атмосферные газы, пыль. Вода появляется на поверхности металла или непосредственно после осадков или в результате конденсации. Здесь определяющая роль у влажности воздуха. Выделяется три случая: мокрая коррозия, влажная и сухая.
При относительной влажности, близкой к 100 %-й в результате конденсации, а так же из-за осадков, на поверхности образуется видимый слой воды или ее капли. Это случай мокрой коррозии.
При влажности воздуха 60–70 % на поверхности появляется невидимая адсорбционная пленка воды (порядка нескольких молекулярных слоев) – влажная коррозия.
При влажности менее 60 % на поверхности вода отсутствует – сухая коррозия. Сразу отметим, что она носит химический характер (см. далее). На поверхности металлов при реакции с кислородом образуется защитная оксидная пленка (металл лишь тускнеет). Скорость химической атмосферной коррозии невелика (из-за невысоких температур) по сравнению с остальными видами. Существенной роли она не играет.
Когда поверхность влажная (появляется электролит) скорость коррозии уже существенна. Коррозия при этом носит электрохимический характер. Рассмотрим реакции при атмосферной коррозии железа с кислородной деполяризацией
(–) А Fe | Н2O, O2 | Fe (O2) K(+)
А(–) Fe– 2ē→ Fе2+
К(+) О2 + 4ē + 2Н2О → 4ОН-
___________________________
2Fe + О2+ 2Н2О = 2Fe(ОН)2.
Первичный продукт коррозии Fe(ОН)2 светло-зеленоватого цвета неустойчив и быстро доокисляетсядо коричневатого Fe(ОН)3
4Fe(ОН)2 + О2+ 2Н2О = 4Fe(ОН)3
и затем превращается в ржавчину – гидрат оксидов железа переменного состава х
FeО
·y
Fe2О3
·z
Н2О.
В случаи влажной коррозии, когда кислород легко проникает через пленку воды, процесс контролируется анодной реакцией и омической составляющей
среды. При мокрой коррозии наблюдается катодное торможение, так как доступ кислорода через утолщенные пленки затруднен.
Далее рассмотрим основные специфические факторы, которые увеличивают скорость атмосферной коррозии.
1. Повышение влажности атмосферы. Как уже отмечалось, увеличение
влажности более 60 % приводит к конденсации воды и, следовательно, к возрастанию коррозии. На влажность влияет погодный фактор. В определенные времена года увеличивается продолжительность и число циклов смачивания. Осенью (в более дождливый период) коррозия интенсивней, чем летом. В зимний период при отрицательных температурах на поверхностях вообще отсутствует жидкая вода и коррозией можно пренебречь.
2. Температура может действовать двояко. При повышенной влажности
(например, во время дождливого времени года в тропических зонах) повышение температуры значительно ускоряет коррозию. При переходе весной от отрицательных к положительным температурам коррозия увеличивается. Но часто повышение температуры тормозит коррозию: падает влажность воздуха, высыхает поверхность металлов, снижается растворимость кислорода в воде.
3. Значительное влияние оказывает загрязнение воздуха различными газа-
ми, пылью, дымом. Это меняет состав влажной пленки на поверхности и ускоряет коррозию в десятки раз. Наиболее агрессивные газы: SО2, NО2, HCl, H2S. При растворении в воде они создают кислую среду, разрушающую защитные пленки. Сероводород H2S опасен для серебра (электротехника). Аммиак NН3 в воде дает щелочную среду (опасен для алюминия, цинка, свинца, олова) и хороший комплексообразователь (опасен для меди). В прибрежных морских районах воздух содержит агрессивные хлориды солей. Пыль, оседая на поверхность, способствует конденсации и удерживанию влаги. Чистый влажный воздух не так опасен. Так, если в относительно чистой атмосфере сельских районов скорость коррозии обычных сталей составляет около 0,1–0,15 мм/год, то в промышленной сильно загрязненной атмосфере 0,45–0,5 мм/год.
В среднем скорость атмосферной коррозии в городских условиях для различных металлов составляет по возрастанию, в мм/год: 0,004 Pb; 0,008 Al; 0,012 Cu и Sn; 0,05 Zn; 0,2 Fe. Интересно, что поверхность меди в присутствии атмосферного СО2 и воды может покрывается зеленоватым налетом из основного карбоната (СuОH)2СО3. К наиболее стойким металлам на воздухе относится Ti, ряд редких металлов (из-за защитных оксидных пленок) и благородные металлы. Но, серебро немного темнеет (аналогично и медь) в присутствии сероводорода
4Ag + O2 + 2H2S = 2Ag2S (черный) + 2H2О.
Почвенная коррозия
Протекает в почве и грунте (грунт под почвой и не содержит органики). Ей подвержены трубопроводы, сваи, резервуары, опоры и др. Коррозия носит электрохимический характер. Механизм ее такой же, как при атмосферной коррозии (в случае невысокой влажности), или в электролитах.
Скорость коррозии металлов зависит от влажности, состава, величины рН и пористости почвы, наличия микроорганизмов. По агрессивности грунты подразделяются на несколько видов. Максимальная коррозия происходит при влажности 15–25 %. Свыше затруднен доступ кислорода из-за насыщения грунта водой. Минерализация почв меняется в широких пределах – от 10 до 300 мг/л разных солей. Оба фактора, а также гранулометрический состав, определяет омическое сопротивление грунта. Чем меньше сопротивление, тем грунты агрессивней (табл. 2.2).
Таблица 2.2
Удельное сопротивление грунта и его коррозионная агрессивность
| Удел.соп- ротивление, Ом· м | <5 | 5-10 | 10-20 | 20-100 | >100 | |
| Агрессив- ность грунта | Особо высокая | Высокая | Повышенная | Средняя | Низкая |
Кислые болотистые и гумусовые почвы с рН = 3–6 отличаются высокой агрессивностью. Здесь окислителем является и Н+, иO2. Встречаются и щелочные почвы – суглинки и солончаки с рН = 7,5–9,5, с окислителем кислородом. У большинства почв значение рН составляет 6–7,5. Большое значение имеет воздухопроницаемость почв: чем она выше, тем больше коррозия. По этой причине песчаные почвы часто более агрессивны, чем глинистые. При сочетании песчаных и глинистых участков очень опасна дифференциальная аэрация. В некоторых случаях анодные и катодные участки могут находиться далеко друг от друга. Так, на трубах (рис. 2.13) на расстоянии до 2 км могут возникать макрогальванические элементы с разностью потенциалов 0,5 В, приводящие значительному питтингообразованию.
Рис. 2.13. Схема коррозионного макрогальванического элемента
подземного трубопровода при различном доступе кислорода
Там, где доступ кислорода облегчен (песчаный участок) – катодный участок, где затруднен (глина) – анодный. Коррозия сваи с учетом грунтовых вод показана на рис. 2.14.
Рис. 2.14. Коррозия стальной сваи в грунте: 1
– верхний слой грунта с большим содержанием кислорода;
2
– катодный участок сваи;
3
– уровень грун-
товых вод; 4
– анодный участок с продуктами коррозии
И в целом, из-за недостаточного поступления кислорода, почвенная коррозия носит местный (локальный) характер. Это приводит к скважному ржавлению в местах язв и питтингов.
Коррозия блуждающими токами (электрокоррозия) и защита
Выделяется в отдельный вид из-за специфичности. Возникает в земле при протекании токов утечки от источников постоянного
тока: вблизи электрифицированных железных дорог (наиболее опасна), линий трамваев, электролизных производств и даже сварочных установок.
При прохождении электровоза часть рельсового тока из-за неполной изоляции стекает (ответвляется) в землю (рис. 2.15).
Рис. 2.15. Возникновение блуждающих токов вблизи ж /д
Если в зоне блуждающих токов оказываются металлические сооружения (труба и др.), то они становятся частью цепи и подвергаются коррозии (часто усиленной). Точная схема токов утечек сложна и зависит от ряда факторов: загрязнения и влажности балласта насыпи; электропроводности самой земли (иногда токи распространяются на многие километры от дороги); удаленности тяговой подстанции, куда в итоге возвращается ток (у трамвайных линий тяговые подстанции располагаются близко друг от друга, и токи утечек не так велики, как на ж/д); мощности локомотива; возможностью смены направления движения; перемещением анодной и катодной зоны и др. Причем можно считать, что за счет внешнего тока происходит электролиз,
поэтому и электрокоррозия. Несколько упрощая, можно дать следующую принципиальную картину процессам.
Анодными зонами с более положительным потенциалом (в обычной коррозии анод отрицательней катода) являются на рельсе места стекания
тока в грунт, а на трубе места
выхода тока
обратно в рельс
А(+) Fe– 2ē→ Fе2+.
И наоборот, катодные зоны для рельса – выход тока из грунта и для трубы –вход тока в трубу с двумя основными реакциями
К(–) 2Н2О + 2ē → Н2+ 2ОН-
О2+ 4ē + 2Н2О → 4ОН-.
Центральная часть трубы составляет нейтральную зону. Для самой железной дороги электрокоррозия наиболее интенсивно наблюдается в тоннелях, где нет проветривания пути от влаги. Так, основная причина замены рельсов в тоннелях – электрокоррозия подошвы рельса.
Главное для уменьшения электрокоррозии – борьба с утечками тока: поддержание в хорошем состоянии балласта и отвод от него воды; прочистка зазоров между балластом и рельсами; электроизоляция рельсов неэлектропроводными прокладками от полотна и шпал; повышение проводимости стыков (хорошее состояние стыковых токовых соединителей, затяжка болтов); применение бесстыкового пути; уменьшения расстояния между тяговыми подстанциями.
Для защиты сооружений вблизи дорог используют электродренаж. Коррозию можно практически исключить, если соединить их проводом с рельсом. Тогда ток пойдет не через грунт и ту же трубу, а через проводник обратно в рельс. Чтобы направление тока не влияло на защиту, в дренажную цепь ставят вентили – диоды. В целом дренаж достаточно сложное техническое решение. Можно использовать и другие способы защиты: катодные станции (см. далее), когда защищаемая конструкция находится на большом расстоянии от дороги (свыше 1км); или протекторы.
2.9. Биокоррозия и защита
Это – коррозия металлов при воздействии микроорганизмов и продуктов их жизнедеятельности. Опасны не бактерии как таковые, а продукты их жизнедеятельности. Микроорганизмы способны вырабатывать не только органические кислоты – муравьиную, уксусную, лимонную, щавелевую, но и сильные неорганические – серную, азотную.
Различают аэробные и анаэробные
микроорганизмы, действие которых на металлы различно.
Аэробные развиваются только в присутствии кислорода. Они подразделяются на тионовые, нитрифицирующие и железобактерии.
Тионовые сначала окисляют соединения серы из почвы (сульфиды, например, FeS2) до серной кислоты, а затем появляется еще ионы трехвалентного железа: FeS2 +O2 + Н2О → Н2SO4 + FeSO4+ O2 → Fe2(SO4)3.
И Н2SO4 и Fe2(SO4)3 окисляют далее металлы. Известен пример влияния биокоррозии при строительстве Киевского метро. Грунтовые воды закислились серной кислотой и стальные конструкции при контакте с ними разрушились за четыре месяца на 40%.
Нитрифицирующие бактерии окисляют аммиак из воздуха и воды до агрессивной азотной кислоты: NH3 +O2 + Н2О → НNO3.
Железобактерии любят поселяться в трубах (в местах неровностей) с проточной водой. Образуя скопления они вызывают кислородную дифференциальную аэрацию при электрохимической коррозии с последующим до окислением двухвалентного железа до трехвалентного: Fe + O2 → Fе2++O2→ Fе3++Fe→ Fе2+ и т.д.
В глубине почвы при низкой концентрации кислорода или без него могут развиваться анаэробные бактерии. Они способны в слабокислой среде восстанавливать сульфат ионы: Fe + SО42-+ H+ → Fе2+ + FeS +H 2S + Н2О.
К методам защиты от биокоррозии относятся следующие. Применение лакокрасочных покрытий с бактерицидными (биоцидными) добавками. Поддержание по возможности оптимальных внешних условий: влажности не более 80 %, температуры не более 20оС. Наличие хорошей вентиляции. Удаление загрязнений (питательной среды) с поверхностей. При необходимости применение электрохимической защиты (протекторной или катодной).
Контактная коррозия
Если, в электролите в контакте находятся металлы с разными потенциалами (разность более 0,25 В), то скорость коррозии их существенно меняется, по-сравнению с отсутствием контакта. Очевидно, что более отрицательный металл будет – анодом и скорость его усилится, а положительный – катодом и коррозия его уменьшится или прекратится. Усиление коррозии одних металлов при контакте с другими принято называть контактной коррозией.
Многие конструкции, машины, приборы нельзя построить из одного металла. Всегда будут в наличии покрытия другими металлами, сварные или паяльные соединения, болты и др. Да и сами сборные конструкции включают применение разных сплавов. В этих случаях нельзя допускать ошибок.
Приведем примеры ошибок. Первый исторический – времен парусного флота. В определенный момент английские корабли получили преимущество в быстроходности над французскими парусниками. Деревянные днища английских судов стали обшивать медными листами. Но через некоторое время листы дорогостоящей меди стали отваливаться в море. Причина – крепление меди осуществлялось железными гвоздями, которые быстро аноднокорродировали. Понятно, что их надо заменить на медные. В ракетостроении (60-е годы) были неприятные ошибки. Например, быстро выходили из строя подшипники, состоящие из латуни и стали. Пришлось все детали в подшипниках хромировать. Или ряд примеров без непосредственного контакта металлов. Стальные и алюминиевые баки для нагрева растворов неожиданно быстро корродировали. Оказалось, что змеевики в них были медные (но, подчеркнем, без прямого контакта). В раствор попадало небольшое количество ионов меди из змеевиков. Далее они восстанавливались на поверхности баков:Cu2+ +Al(Fe) → Cu + Al3+(Fe2+). Образовывались микрогальванические элементы (с катодом из Cu) с дальнейшей усиленной коррозией баков. Еще пример. Титановые листы покрывались налетом ржавчины?! Оказалось, что они подвергались поверхностной очистке стальной дробью. Следы стали оставались в титане и ржавели.
Нельзя соединять напрямую медный провод с алюминиевым на открытом воздухе. В месте контакта алюминий станет анодом и при попадании влаги начнет окисляться. Со временем будет нарушена проводимость. Нежелательно на медь ставить стальной болт (анод). Продукты коррозии могут не позволить его свободно демонтировать.
Рассмотрим совместимость важнейших практических контактных пар металлов при атмосферной коррозии.
Al-сталь, Al-Ti в большинстве случаев контакт допускается (алюминий защищен оксидной пленкой), кроме морского воздуха.Al-Zn, Al-Cd, Al-Pb хорошо совместимы.Al-Cu нельзя использовать, даже при анодированном алюминии.Fe-Niопасная пара для первого.Fe-нержавеющая сталь, Fe-Cu нежелательные пары (особенно в морских условиях).Fe-Pb, Pb-Cu хорошо совместимы.
Если нельзя избежать контактирования, то места соприкосновения надо заизолировать: лаками, смазками, мастиками, полимерными прокладками (шайбы пластмассовые под болты). В электрических контактах используют промежуточный металл: между алюминием и медью прокладывается сталь.
Атмосферная коррозия
Атмосферная коррозия – это коррозия металлов в условиях земной атмосферы (во влажном воздухе и температуре окружающей среды). Она наиболее распространена. Имеет ряд специфических ее особенностей. Коррозионной средой (электролитом) является вода, в которой присутствуют кислород воздуха (окислитель), атмосферные газы, пыль. Вода появляется на поверхности металла или непосредственно после осадков или в результате конденсации. Здесь определяющая роль у влажности воздуха. Выделяется три случая: мокрая коррозия, влажная и сухая.
При относительной влажности, близкой к 100 %-й в результате конденсации, а так же из-за осадков, на поверхности образуется видимый слой воды или ее капли. Это случай мокрой коррозии.
При влажности воздуха 60–70 % на поверхности появляется невидимая адсорбционная пленка воды (порядка нескольких молекулярных слоев) – влажная коррозия.
При влажности менее 60 % на поверхности вода отсутствует – сухая коррозия. Сразу отметим, что она носит химический характер (см. далее). На поверхности металлов при реакции с кислородом образуется защитная оксидная пленка (металл лишь тускнеет). Скорость химической атмосферной коррозии невелика (из-за невысоких температур) по сравнению с остальными видами. Существенной роли она не играет.
Когда поверхность влажная (появляется электролит) скорость коррозии уже существенна. Коррозия при этом носит электрохимический характер. Рассмотрим реакции при атмосферной коррозии железа с кислородной деполяризацией
(–) А Fe | Н2O, O2 | Fe (O2) K(+)
А(–) Fe– 2ē→ Fе2+
К(+) О2 + 4ē + 2Н2О → 4ОН-
___________________________
2Fe + О2+ 2Н2О = 2Fe(ОН)2.
Первичный продукт коррозии Fe(ОН)2 светло-зеленоватого цвета неустойчив и быстро доокисляетсядо коричневатого Fe(ОН)3
4Fe(ОН)2 + О2+ 2Н2О = 4Fe(ОН)3
и затем превращается в ржавчину – гидрат оксидов железа переменного состава х
FeО
·y
Fe2О3
·z
Н2О.
В случаи влажной коррозии, когда кислород легко проникает через пленку воды, процесс контролируется анодной реакцией и омической составляющей
среды. При мокрой коррозии наблюдается катодное торможение, так как доступ кислорода через утолщенные пленки затруднен.
Далее рассмотрим основные специфические факторы, которые увеличивают скорость атмосферной коррозии.
1. Повышение влажности атмосферы. Как уже отмечалось, увеличение
влажности более 60 % приводит к конденсации воды и, следовательно, к возрастанию коррозии. На влажность влияет погодный фактор. В определенные времена года увеличивается продолжительность и число циклов смачивания. Осенью (в более дождливый период) коррозия интенсивней, чем летом. В зимний период при отрицательных температурах на поверхностях вообще отсутствует жидкая вода и коррозией можно пренебречь.
2. Температура может действовать двояко. При повышенной влажности
(например, во время дождливого времени года в тропических зонах) повышение температуры значительно ускоряет коррозию. При переходе весной от отрицательных к положительным температурам коррозия увеличивается. Но часто повышение температуры тормозит коррозию: падает влажность воздуха, высыхает поверхность металлов, снижается растворимость кислорода в воде.
3. Значительное влияние оказывает загрязнение воздуха различными газа-
ми, пылью, дымом. Это меняет состав влажной пленки на поверхности и ускоряет коррозию в десятки раз. Наиболее агрессивные газы: SО2, NО2, HCl, H2S. При растворении в воде они создают кислую среду, разрушающую защитные пленки. Сероводород H2S опасен для серебра (электротехника). Аммиак NН3 в воде дает щелочную среду (опасен для алюминия, цинка, свинца, олова) и хороший комплексообразователь (опасен для меди). В прибрежных морских районах воздух содержит агрессивные хлориды солей. Пыль, оседая на поверхность, способствует конденсации и удерживанию влаги. Чистый влажный воздух не так опасен. Так, если в относительно чистой атмосфере сельских районов скорость коррозии обычных сталей составляет около 0,1–0,15 мм/год, то в промышленной сильно загрязненной атмосфере 0,45–0,5 мм/год.
В среднем скорость атмосферной коррозии в городских условиях для различных металлов составляет по возрастанию, в мм/год: 0,004 Pb; 0,008 Al; 0,012 Cu и Sn; 0,05 Zn; 0,2 Fe. Интересно, что поверхность меди в присутствии атмосферного СО2 и воды может покрывается зеленоватым налетом из основного карбоната (СuОH)2СО3. К наиболее стойким металлам на воздухе относится Ti, ряд редких металлов (из-за защитных оксидных пленок) и благородные металлы. Но, серебро немного темнеет (аналогично и медь) в присутствии сероводорода
4Ag + O2 + 2H2S = 2Ag2S (черный) + 2H2О.
Почвенная коррозия
Протекает в почве и грунте (грунт под почвой и не содержит органики). Ей подвержены трубопроводы, сваи, резервуары, опоры и др. Коррозия носит электрохимический характер. Механизм ее такой же, как при атмосферной коррозии (в случае невысокой влажности), или в электролитах.
Скорость коррозии металлов зависит от влажности, состава, величины рН и пористости почвы, наличия микроорганизмов. По агрессивности грунты подразделяются на несколько видов. Максимальная коррозия происходит при влажности 15–25 %. Свыше затруднен доступ кислорода из-за насыщения грунта водой. Минерализация почв меняется в широких пределах – от 10 до 300 мг/л разных солей. Оба фактора, а также гранулометрический состав, определяет омическое сопротивление грунта. Чем меньше сопротивление, тем грунты агрессивней (табл. 2.2).
Таблица 2.2
Удельное сопротивление грунта и его коррозионная агрессивность
| Удел.соп- ротивление, Ом· м | <5 | 5-10 | 10-20 | 20-100 | >100 | |
| Агрессив- ность грунта | Особо высокая | Высокая | Повышенная | Средняя | Низкая |
Кислые болотистые и гумусовые почвы с рН = 3–6 отличаются высокой агрессивностью. Здесь окислителем является и Н+, иO2. Встречаются и щелочные почвы – суглинки и солончаки с рН = 7,5–9,5, с окислителем кислородом. У большинства почв значение рН составляет 6–7,5. Большое значение имеет воздухопроницаемость почв: чем она выше, тем больше коррозия. По этой причине песчаные почвы часто более агрессивны, чем глинистые. При сочетании песчаных и глинистых участков очень опасна дифференциальная аэрация. В некоторых случаях анодные и катодные участки могут находиться далеко друг от друга. Так, на трубах (рис. 2.13) на расстоянии до 2 км могут возникать макрогальванические элементы с разностью потенциалов 0,5 В, приводящие значительному питтингообразованию.
Рис. 2.13. Схема коррозионного макрогальванического элемента
подземного трубопровода при различном доступе кислорода
Там, где доступ кислорода облегчен (песчаный участок) – катодный участок, где затруднен (глина) – анодный. Коррозия сваи с учетом грунтовых вод показана на рис. 2.14.
Рис. 2.14. Коррозия стальной сваи в грунте: 1
– верхний слой грунта с большим содержанием кислорода;
2
– катодный участок сваи;
3
– уровень грун-
товых вод; 4
– анодный участок с продуктами коррозии
И в целом, из-за недостаточного поступления кислорода, почвенная коррозия носит местный (локальный) характер. Это приводит к скважному ржавлению в местах язв и питтингов.
Коррозия блуждающими токами (электрокоррозия) и защита
Выделяется в отдельный вид из-за специфичности. Возникает в земле при протекании токов утечки от источников постоянного
тока: вблизи электрифицированных железных дорог (наиболее опасна), линий трамваев, электролизных производств и даже сварочных установок.
При прохождении электровоза часть рельсового тока из-за неполной изоляции стекает (ответвляется) в землю (рис. 2.15).
Рис. 2.15. Возникновение блуждающих токов вблизи ж /д
Если в зоне блуждающих токов оказываются металлические сооружения (труба и др.), то они становятся частью цепи и подвергаются коррозии (часто усиленной). Точная схема токов утечек сложна и зависит от ряда факторов: загрязнения и влажности балласта насыпи; электропроводности самой земли (иногда токи распространяются на многие километры от дороги); удаленности тяговой подстанции, куда в итоге возвращается ток (у трамвайных линий тяговые подстанции располагаются близко друг от друга, и токи утечек не так велики, как на ж/д); мощности локомотива; возможностью смены направления движения; перемещением анодной и катодной зоны и др. Причем можно считать, что за счет внешнего тока происходит электролиз,
поэтому и электрокоррозия. Несколько упрощая, можно дать следующую принципиальную картину процессам.
Анодными зонами с более положительным потенциалом (в обычной коррозии анод отрицательней катода) являются на рельсе места стекания
тока в грунт, а на трубе места
выхода тока
обратно в рельс
А(+) Fe– 2ē→ Fе2+.
И наоборот, катодные зоны для рельса – выход тока из грунта и для трубы –вход тока в трубу с двумя основными реакциями
К(–) 2Н2О + 2ē → Н2+ 2ОН-
О2+ 4ē + 2Н2О → 4ОН-.
Центральная часть трубы составляет нейтральную зону. Для самой железной дороги электрокоррозия наиболее интенсивно наблюдается в тоннелях, где нет проветривания пути от влаги. Так, основная причина замены рельсов в тоннелях – электрокоррозия подошвы рельса.
Главное для уменьшения электрокоррозии – борьба с утечками тока: поддержание в хорошем состоянии балласта и отвод от него воды; прочистка зазоров между балластом и рельсами; электроизоляция рельсов неэлектропроводными прокладками от полотна и шпал; повышение проводимости стыков (хорошее состояние стыковых токовых соединителей, затяжка болтов); применение бесстыкового пути; уменьшения расстояния между тяговыми подстанциями.
Для защиты сооружений вблизи дорог используют электродренаж. Коррозию можно практически исключить, если соединить их проводом с рельсом. Тогда ток пойдет не через грунт и ту же трубу, а через проводник обратно в рельс. Чтобы направление тока не влияло на защиту, в дренажную цепь ставят вентили – диоды. В целом дренаж достаточно сложное техническое решение. Можно использовать и другие способы защиты: катодные станции (см. далее), когда защищаемая конструкция находится на большом расстоянии от дороги (свыше 1км); или протекторы.
2.9. Биокоррозия и защита
Это – коррозия металлов при воздействии микроорганизмов и продуктов их жизнедеятельности. Опасны не бактерии как таковые, а продукты их жизнедеятельности. Микроорганизмы способны вырабатывать не только органические кислоты – муравьиную, уксусную, лимонную, щавелевую, но и сильные неорганические – серную, азотную.
Различают аэробные и анаэробные
микроорганизмы, действие которых на металлы различно.
Аэробные развиваются только в присутствии кислорода. Они подразделяются на тионовые, нитрифицирующие и железобактерии.
Тионовые сначала окисляют соединения серы из почвы (сульфиды, например, FeS2) до серной кислоты, а затем появляется еще ионы трехвалентного железа: FeS2 +O2 + Н2О → Н2SO4 + FeSO4+ O2 → Fe2(SO4)3.
И Н2SO4 и Fe2(SO4)3 окисляют далее металлы. Известен пример влияния биокоррозии при строительстве Киевского метро. Грунтовые воды закислились серной кислотой и стальные конструкции при контакте с ними разрушились за четыре месяца на 40%.
Нитрифицирующие бактерии окисляют аммиак из воздуха и воды до агрессивной азотной кислоты: NH3 +O2 + Н2О → НNO3.
Железобактерии любят поселяться в трубах (в местах неровностей) с проточной водой. Образуя скопления они вызывают кислородную дифференциальную аэрацию при электрохимической коррозии с последующим до окислением двухвалентного железа до трехвалентного: Fe + O2 → Fе2++O2→ Fе3++Fe→ Fе2+ и т.д.
В глубине почвы при низкой концентрации кислорода или без него могут развиваться анаэробные бактерии. Они способны в слабокислой среде восстанавливать сульфат ионы: Fe + SО42-+ H+ → Fе2+ + FeS +H 2S + Н2О.
К методам защиты от биокоррозии относятся следующие. Применение лакокрасочных покрытий с бактерицидными (биоцидными) добавками. Поддержание по возможности оптимальных внешних условий: влажности не более 80 %, температуры не более 20оС. Наличие хорошей вентиляции. Удаление загрязнений (питательной среды) с поверхностей. При необходимости применение электрохимической защиты (протекторной или катодной).
Контактная коррозия
Если, в электролите в контакте находятся металлы с разными потенциалами (разность более 0,25 В), то скорость коррозии их существенно меняется, по-сравнению с отсутствием контакта. Очевидно, что более отрицательный металл будет – анодом и скорость его усилится, а положительный – катодом и коррозия его уменьшится или прекратится. Усиление коррозии одних металлов при контакте с другими принято называть контактной коррозией.
Многие конструкции, машины, приборы нельзя построить из одного металла. Всегда будут в наличии покрытия другими металлами, сварные или паяльные соединения, болты и др. Да и сами сборные конструкции включают применение разных сплавов. В этих случаях нельзя допускать ошибок.
Приведем примеры ошибок. Первый исторический – времен парусного флота. В определенный момент английские корабли получили преимущество в быстроходности над французскими парусниками. Деревянные днища английских судов стали обшивать медными листами. Но через некоторое время листы дорогостоящей меди стали отваливаться в море. Причина – крепление меди осуществлялось железными гвоздями, которые быстро аноднокорродировали. Понятно, что их надо заменить на медные. В ракетостроении (60-е годы) были неприятные ошибки. Например, быстро выходили из строя подшипники, состоящие из латуни и стали. Пришлось все детали в подшипниках хромировать. Или ряд примеров без непосредственного контакта металлов. Стальные и алюминиевые баки для нагрева растворов неожиданно быстро корродировали. Оказалось, что змеевики в них были медные (но, подчеркнем, без прямого контакта). В раствор попадало небольшое количество ионов меди из змеевиков. Далее они восстанавливались на поверхности баков:Cu2+ +Al(Fe) → Cu + Al3+(Fe2+). Образовывались микрогальванические элементы (с катодом из Cu) с дальнейшей усиленной коррозией баков. Еще пример. Титановые листы покрывались налетом ржавчины?! Оказалось, что они подвергались поверхностной очистке стальной дробью. Следы стали оставались в титане и ржавели.
Нельзя соединять напрямую медный провод с алюминиевым на открытом воздухе. В месте контакта алюминий станет анодом и при попадании влаги начнет окисляться. Со временем будет нарушена проводимость. Нежелательно на медь ставить стальной болт (анод). Продукты коррозии могут не позволить его свободно демонтировать.
Рассмотрим совместимость важнейших практических контактных пар металлов при атмосферной коррозии.
Al-сталь, Al-Ti в большинстве случаев контакт допускается (алюминий защищен оксидной пленкой), кроме морского воздуха.Al-Zn, Al-Cd, Al-Pb хорошо совместимы.Al-Cu нельзя использовать, даже при анодированном алюминии.Fe-Niопасная пара для первого.Fe-нержавеющая сталь, Fe-Cu нежелательные пары (особенно в морских условиях).Fe-Pb, Pb-Cu хорошо совместимы.
Если нельзя избежать контактирования, то места соприкосновения надо заизолировать: лаками, смазками, мастиками, полимерными прокладками (шайбы пластмассовые под болты). В электрических контактах используют промежуточный металл: между алюминием и медью прокладывается сталь.
Методы защиты от коррозии металла
Основной способ защиты от коррозии металла – это создание защитных покрытий – металлических, неметаллических или химических.
Металлические покрытия
Металлическое покрытие наносится на металл, который нужно защитить от коррозии, слоем другого металла, устойчивого к коррозии в тех же условиях. Если металлическое покрытие изготовлено из металла с более отрицательным потенциалом (более активный) , чем защищаемый, то оно называется анодным покрытием. Если металлическое покрытие изготовлено из металла с более положительным потенциалом (менее активный), чем защищаемый, то оно называется катодным покрытием.
Например, при нанесении слоя цинка на железо, при нарушении целостности покрытия, цинк выступает в качестве анода и будет разрушаться, а железо защищено до тех пор, пока не израсходуется весь цинк. Цинковое покрытие является в данном случае анодным.
Катодным покрытием для защиты железа, может, например, быть медь или никель. При нарушении целостности такого покрытия, разрушается защищаемый металл.
Неметаллические покрытия
Такие покрытия могут быть неорганические (цементный раствор, стекловидная масса) и органические (высокомолекулярные соединения, лаки, краски, битум).
Химические покрытия
В этом случае защищаемый металл подвергают химической обработке с целью образования на поверхности пленки его соединения, устойчивой к коррозии. Сюда относятся:
оксидирование – получение устойчивых оксидных пленок (Al2O3, ZnO и др.);
фосфатирование – получение защитной пленки фосфатов (Fe3(PO4)2, Mn3(PO4)2);
азотирование – поверхность металла (стали) насыщают азотом;
воронение стали – поверхность металла взаимодействует с органическими веществами;
цементация – получение на поверхности металла его соединения с углеродом.
Изменение состава технического металла и коррозионной среды
Изменение состава технического металла также способствует повышению стойкости металла к коррозии. В этом случае в металл вводят такие соединения, которые увеличивают его коррозионную стойкость.
Изменение состава коррозионной среды (введение ингибиторов коррозии или удаление примесей из окружающей среды) тоже является средством защиты металла от коррозии.
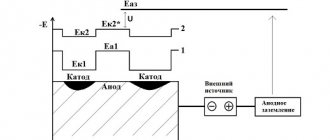
Электрохимическая защита
Электрохимическая защита основывается на присоединении защищаемого сооружения катоду внешнего источника постоянного тока, в результате чего оно становится катодом. Анодом служит металлический лом, который разрушаясь, защищает сооружение от коррозии.
Протекторная защита – один из видов электрохимической защиты – заключается в следующем.
К защищаемому сооружению присоединяют пластины более активного металла, который называется протектором. Протектор – металл с более отрицательным потенциалом – является анодом, а защищаемое сооружение – катодом. Соединение протектора и защищаемого сооружения проводником тока, приводит к разрушению протектора.
Примеры задач с решениями на определение защитных свойств оксидных пленок, определение коррозионной стойкости металлов, а также уравнения реакций, протекающих при электрохимической коррозии металлов приведены в разделе Задачи к разделу Коррозия металлов
Категории Коррозия металлов, ОБЩАЯ ХИМИЯ
Катодная защита
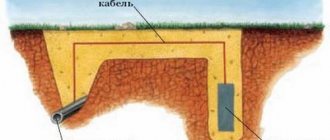
Реализация принципа катодной защиты может осуществляться одним из двух способов. Первый — подача отрицательного потенциала может происходить от специального источника электроэнергии, именуемого станцией катодной защиты.
При использовании катодных станций может возникнуть следующая проблема.
Электричество для установки требуемого потенциала нередко подается по длинному кабелю. Этот кабель подвержен действию молнии и некоторым другим электромагнитным влияниям. Для того, чтобы в результате не произошло перенапряжения, рекомендуется использовать комплексное решение ZANDZ.