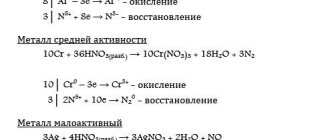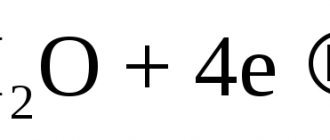Определение коррозии
Материалы из металлов под химическим или электрохимическим воздействием окружающей среды подвергаются разрушению, которое называется коррозией.
Коррозия металлов вызывается окислительно-восстановительными реакциями, в результате которых металлы переходят в окисленную форму и теряют свои свойства, что приводит в негодность металлические материалы.
Можно выделить 3 признака, характеризующих коррозию:
- Коррозия – это с химической точки зрения процесс окислительно-восстановительный.
- Коррозия – это самопроизвольный процесс, возникающий по причине неустойчивости термодинамической системы металл – компоненты окружающей среды.
- Коррозия – это процесс, который развивается в основном на поверхности металла. Однако, не исключено, что коррозия может проникнуть и вглубь металла.
Виды коррозии металлов
Наиболее часто встречаются следующие виды коррозии металлов:
- Равномерная – охватывает всю поверхность равномерно
- Неравномерная
- Избирательная
- Местная пятнами – корродируют отдельные участки поверхности
- Язвенная (или питтинг)
- Точечная
- Межкристаллитная – распространяется вдоль границ кристалла металла
- Растрескивающая
- Подповерхностная
Основные виды коррозии металлов
С точки зрения механизма коррозионного процесса можно выделить два основных типа коррозии: химическую и электрохимическую.
Типы ржавчины
В большей степени коррозии подвержено железо. С точки зрения химии ржавчина — это окислительный процесс (как и горение). Элементы возникающие при окислении в кислородной среде называются Оксиды. Можно выделить 4 основных типа.
1. Желтая ржавчина — химическая формула FeO(OH)H2O (оксид железа двухвалетный). Возникает во влажной, недонасыщенной кислородом среде. Часто встречается под водой. В природе существует в виде минерала вюстита, при этом являясь монооксидом (те содержит 1 атом кислорода).
2. Коричневая ржавчина — Fe2O3 (двойной оксид железа): растет без воды и встречается редко.
3. Черная ржавчина — Fe3O4 (оксид железа четырех валентый). Образуется при малом содержании кислорода и без воды поэтому стабильна и распространяется очень медленно. Этот оксид является ферромагнетиком (при определенных условиях обладает намагниченностью в отсутствие внешнего магнитного поля), поэтому потенциально применим для создания сверх-проводников.
4. Красная ржавчина — химическая формула Fe2O3•H2O (оксид железа трехвалентный). Возникает под воздействием кислорода и воды, самый частый тип, процесс протекает равномерно и затрагивает всю поверхность. В отличии от всех вышеперечисленных не столь опасных для железа видов окисления этот в своей толще образует гидроксид железа, который, начиная отслаиваться, открывает для разрушения все новые слои металла. Реакция может продолжатся до полного разрушения конструкции. Применяется при выплавке чугуна и как краситель в пищевой промышленности. Встречается в природе в естественном виде под названием гематид.
Несколько видов ржавления могут протекать одновременно, не особо мешая друг другу.
Химическая и электрохимическая коррозия
Железо ржавеет, если в нем есть добавки и примеси (например, углерод) и при этом контактирует с водой и кислородом. Если же в воде растворена соль (хлорида натрия и калия), реакция становится электрохимической и процесс ржавления ускоряется. Массовое применение этих солей как в бытовой химии так и для борьбы с льдом и снегом делают электрохимическую коррозию очень распространенным и опасным явлением: потери в США от использования солей в зимний период составляют 2,5 млрд. долларов. При одновременном воздействии воды и кислорода образуется гидроксид железа, который, в отличие от оксида, отслаивается от металла и никак его не защищает. Реакция продолжается либо до полного разрушения железа, либо пока в системе не закончится вода или кислород.
Электрохимическую коррозию могут вызывать блуждающие токи, возникающие при утечке из электрической цепи части тока в водные растворы или в почву и оттуда — в конструкции из металла. В тех местах, где блуждающие токи выходят из металлоконструкций обратно в воду или в почву, происходит разрушение металлов. Особенно часто блуждающие токи возникают в местах движения наземного электротранспорта (например, трамваев и ж/д локомотивов на электрической тяге). Всего за год блуждающие токи силой в 1А способны растворить железа — 9,1 кг, цинка — 10,7 кг, свинца — 33,4 кг.
Во второй части статьи мы расскажем, как вы можете защитить свои металлоконструкции от этой напасти или победить ее, если она уже атакует.
Электрохимическая коррозия металлов
Электрохимическая коррозия металлов – это процесс разрушения металлов в среде различных электролитов, который сопровождается возникновением внутри системы электрического тока.
При таком типе коррозии атом удаляется из кристаллической решетки результате двух сопряженных процессов:
- Анодного – металл в виде ионов переходит в раствор.
- Катодного – образовавшиеся при анодном процессе электроны, связываются деполяризатором (вещество — окислитель).
Сам процесс отвода электронов с катодных участков называется деполяризацией, а вещества способствующие отводу – деполяризаторами.
Наибольшее распространение имеет коррозия металлов с водородной и кислородной деполяризацией.
Водородная деполяризация
Водородная деполяризация осуществляется на катоде при электрохимической коррозии в кислой среде:
2H++2e— = H2 разряд водородных ионов
2H3O++2e— = H2 + 2H2O
Кислородная деполяризация
Кислородная деполяризация осуществляется на катоде при электрохимической коррозии в нейтральной среде:
O2 + 4H++4e— = H2O восстановление растворенного кислорода
O2 + 2H2O + 4e— = 4OH—
Все металлы, по их отношению к электрохимической коррозии, можно разбить на 4 группы, которые определяются величинами их стандартных электродных потенциалов:
- Активные металлы (высокая термодинамическая нестабильность) – это все металлы, находящиеся в интервале щелочные металлы — кадмий (Е0 = -0,4 В). Их коррозия возможна даже в нейтральных водных средах, в которых отсутствуют кислород или другие окислители.
- Металлы средней активности (термодинамическая нестабильность) – располагаются между кадмием и водородом (Е0 = 0,0 В). В нейтральных средах, в отсутствии кислорода, не корродируют, но подвергаются коррозии в кислых средах.
- Малоактивные металлы (промежуточная термодинамическая стабильность) – находятся между водородом и родием (Е0 = +0,8 В). Они устойчивы к коррозии в нейтральных и кислых средах, в которых отсутствует кислород или другие окислители.
- Благородные металлы (высокая термодинамическая стабильность) – золото, платина, иридий, палладий. Могут подвергаться коррозии лишь в кислых средах при наличии в них сильных окислителей.
Виды электрохимической коррозии
Электрохимическая коррозия может протекать в различных средах. В зависимости от характера среды выделяют следующие виды электрохимической коррозии:
- Коррозия в растворах электролитов — в растворах кислот, оснований, солей, в природной воде.
- Атмосферная коррозия – в атмосферных условиях и в среде любого влажного газа. Это самый распространенный вид коррозии.
Например, при взаимодействии железа с компонентами окружающей среды, некоторые его участки служат анодом, где происходит окисление железа, а другие – катодом, где происходит восстановление кислорода:
А: Fe – 2e— = Fe2+
K: O2 + 4H+ + 4e— = 2H2O
Катодом является та поверхность, где больше приток кислорода.
- Почвенная коррозия – в зависимости от состава почв, а также ее аэрации, коррозия может протекать более или менее интенсивно. Кислые почвы наиболее агрессивны, а песчаные – наименее.
- Аэрационная коррозия — возникает при неравномерном доступе воздуха к различным частям материала.
- Морская коррозия – протекает в морской воде, в связи с наличием в ней растворенных солей, газов и органических веществ.
- Биокоррозия – возникает в результате жизнедеятельности бактерий и других организмов, вырабатывающих такие газы как CO2, H2S и др., способствующие коррозии металла.
- Электрокоррозия – происходит под действием блуждающих токов на подземных сооружениях, в результате работ электрических железных дорог, трамвайных линий и других агрегатов.
Методы защиты от коррозии металла
Основной способ защиты от коррозии металла – это создание защитных покрытий – металлических, неметаллических или химических.
Металлические покрытия
Металлическое покрытие наносится на металл, который нужно защитить от коррозии, слоем другого металла, устойчивого к коррозии в тех же условиях. Если металлическое покрытие изготовлено из металла с более отрицательным потенциалом (более активный) , чем защищаемый, то оно называется анодным покрытием. Если металлическое покрытие изготовлено из металла с более положительным потенциалом (менее активный), чем защищаемый, то оно называется катодным покрытием.
Например, при нанесении слоя цинка на железо, при нарушении целостности покрытия, цинк выступает в качестве анода и будет разрушаться, а железо защищено до тех пор, пока не израсходуется весь цинк. Цинковое покрытие является в данном случае анодным.
Катодным покрытием для защиты железа, может, например, быть медь или никель. При нарушении целостности такого покрытия, разрушается защищаемый металл.
Неметаллические покрытия
Такие покрытия могут быть неорганические (цементный раствор, стекловидная масса) и органические (высокомолекулярные соединения, лаки, краски, битум).
Химические покрытия
В этом случае защищаемый металл подвергают химической обработке с целью образования на поверхности пленки его соединения, устойчивой к коррозии. Сюда относятся:
оксидирование – получение устойчивых оксидных пленок (Al2O3, ZnO и др.);
фосфатирование – получение защитной пленки фосфатов (Fe3(PO4)2, Mn3(PO4)2);
азотирование – поверхность металла (стали) насыщают азотом;
воронение стали – поверхность металла взаимодействует с органическими веществами;
цементация – получение на поверхности металла его соединения с углеродом.
Изменение состава технического металла и коррозионной среды
Изменение состава технического металла также способствует повышению стойкости металла к коррозии. В этом случае в металл вводят такие соединения, которые увеличивают его коррозионную стойкость.
Изменение состава коррозионной среды (введение ингибиторов коррозии или удаление примесей из окружающей среды) тоже является средством защиты металла от коррозии.
Электрохимическая защита
Электрохимическая защита основывается на присоединении защищаемого сооружения катоду внешнего источника постоянного тока, в результате чего оно становится катодом. Анодом служит металлический лом, который разрушаясь, защищает сооружение от коррозии.
Протекторная защита – один из видов электрохимической защиты – заключается в следующем.
К защищаемому сооружению присоединяют пластины более активного металла, который называется протектором. Протектор – металл с более отрицательным потенциалом – является анодом, а защищаемое сооружение – катодом. Соединение протектора и защищаемого сооружения проводником тока, приводит к разрушению протектора.
Примеры задач с решениями на определение защитных свойств оксидных пленок, определение коррозионной стойкости металлов, а также уравнения реакций, протекающих при электрохимической коррозии металлов приведены в разделе Задачи к разделу Коррозия металлов
Категории Коррозия металлов, ОБЩАЯ ХИМИЯ
Способы удаления ржавчины
Народная мудрость гласит, что любую проблему проще предотвратить, чем потом прикладывать героические усилия для устранения ее последствий. Ржавчина – не исключение. За последние 20-30 лет химики и физики предложили немало способов предотвращения коррозии – от защитных покрытий до сложных инженерных сооружений – станций электрохимической защиты.
Если ржавчина все-таки появилась – это не повод опускать руки: есть немало эффективных способов ее удаления, и чем раньше предприняты активные меры, тем большим будет эффект от их применения. Итак, обо всем по порядку.
Механическое удаление ржавчины
Продукты коррозии обладают малой адгезией и поэтому легко удаляются с поверхности металла при механическом воздействии – например, при обработке металлической щеткой. Снять ржавый налет с крупных изделий можно с помощью шлифовального станка, соблюдая при этом простое правило: начинать нужно с крупного зерна, а для финишной обработки использовать самое мелкое. Участки металла, с которых удалена ржавчина, оказываются совершенно беззащитными перед атмосферным воздействием. Если их не обработать антикоррозионными составами, предотвращающими контакт с водой и кислородом, процесс ржавления только ускорится.
Химические способы удаления ржавчины
Зная природу и химический состав ржавчины, логично предположить, что удалить ее можно с помощью кислот. Из школьного курса химии известно, что оксиды и гидроксиды металлов легко взаимодействуют с кислотами, при этом образуются соли железа и соответствующей кислоты, и вода.
Например, при действии соляной кислоты происходят следующие реакции:
- 2Fe (OH)3 + 6HCL → 2FeCl3 + 6H2O
- Fe (OH)2 + 2HCL → FeCl2 +2H2O
Образующийся хлорид железа – водорастворимая соль, которую необходимо удалить с поверхности обрабатываемого изделия простым ополаскиванием в воде, а затем насухо вытереть поверхность. Не надо ждать, пока ржавчина начнет образовываться снова, очищенные участки следует обработать защитными составами.
При обработке кислотами существует опасность растворения металла, поскольку железо в электрохимическом ряду напряжений стоит до водорода, оно активно реагирует со многими разбавленными кислотами:
- Fe + 2HCl → FeCl2 + H2↑
По этой причине прежде, чем заняться химическими экспериментами в домашних условиях, необходимо почитать соответствующую литературу. Устранить побочный эффект поможет ингибитор коррозии – уротропин, при добавлении всего 1-2 г на литр раствора соляной кислоты реакция с железом не протекает.
Преобразователи ржавчины
Жидкие составы на основе ортофосфорной кислоты являются отличным способом предотвратить дальнейшее образование ржавчины на поверхности стальных и железных изделий. При таком способе обработки предварительно удаляются лишь те участки ржавчины, которые слабо держатся на основе. Образующийся в процессе реакции ортофосфат железа создает прочную защитную пленку, через которую не проникает влага и кислород, благодаря чему предотвращается дальнейшая коррозия металла. Для ускорения процесса высыхания на литр 25%-ого раствора ортофосфорной кислоты можно добавить 30-40 мл изобутилового спирта или 15 граммов винной кислоты.
Современное оборудование для удаления ржавчины
Механические способы очистки поверхности от ржавчины с помощью подручных средств применимы далеко не всегда, если изделие имеет сложную форму, то обработать все участки не представляется возможным. Химические способы тоже имеют свои недостатки, при несоблюдении элементарных правил техники безопасности можно получить химический ожог или отравление. Определенную проблему представляет и утилизация отработанных растворов.
Оптимальным способом удаления ржавчины, особенно с поверхности изделий сложной геометрической формы, является мягкий бластинг. Суть метода состоит в следующем, на металлическое изделие направляется струя сжатого воздуха, содержащая особые абразивные гранулы. Меняя давление, можно регулировать глубину слоя, снимаемого с поверхности – таким образом удаляется только слой ржавчины или окалины, а металл остается нетронутым. Гранулы ARMEX, используемые в аппарате для мягкого бластинга Nordblast NB 28-2, состоят из мельчайших частиц соды и мела. Попадая под большим давлением на поверхность, они легко удаляют не только ржавчину, но и лакокрасочные материалы.
Отличительной особенностью метода является абсолютная экологическая безопасность: применяемые компоненты химически инертны. Многочисленные исследования доказали, что на поверхности металла практически не образуются царапины и иные микроскопические дефекты, которые последствии могут стать центрами повторного образования ржавчины. Щелочная природа гранул способствует образованию пассивной пленки на изделиях из железа или стали, предохраняя основной объем металла от коррозионного разрушения.
Наилучшие результаты применения аппарата мягкого бластинга Nordblast NB 28-2 получены при обработке деталей машин или яхт. Процесс чистки от ржавчины зависит от степени коррозии, обычно на полную обработку автомобиля уходит 1 день, яхты – 2 дня.
Чем раньше обнаружена проблема, тем проще бороться с ржавчиной. Какой способ наиболее предпочтителен – каждый решает самостоятельно, но не стоит пользоваться дедовскими методами, если есть оборудование, удаляющее ржавчину со 100%-ой эффективностью!