Алюминий и его реакция с водой
Впервые алюминий был получен лишь в начале XIX века. Cделал это физик Ганс Эрстед. Свой эксперимент он проводил с амальгамой калия, хлоридом алюминия и ртутью.
Кстати, название этого серебристого материала произошло от латинского слова «квасцы», потому что именно из них добывается этот элемент.
Квасцы [Wikimedia]
Квасцы – это природные минералы на основе металлов, которые объединяют в своем составе соли серной кислоты.
Раньше алюминий считался драгоценным металлом и стоил на порядок дороже, чем золото. Объяснялось это тем, что металл было довольно сложно отделить от примесей. Так что позволить себе украшения из алюминия могли только богатые и влиятельные люди.
Японское украшение из алюминия [Wikimedia]
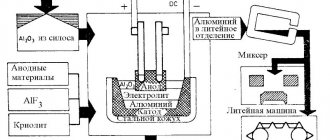
Но в 1886 году Чарльз Холл придумал метод по добыче алюминия в промышленном масштабе, что резко удешевило этот металл и позволило применять его в металлургическом производстве. Промышленный метод заключался в электролизе расплава криолита, в котором растворен оксид алюминия.
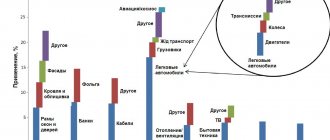
Алюминий — очень востребованный металл, ведь именно из него изготавливаются многие вещи, которыми человек пользуется в быту.
Применение алюминия
Благодаря ковкости и легкости, а также защищенности от коррозии, алюминий является ценным металлом в современной промышленности. Из алюминия изготавливают не только кухонную посуду — он широко используется в авто- и авиастроительстве.
Также алюминий является одним из самых недорогих и экономичных материалов, так как его можно использовать бесконечно, переплавляя ненужные алюминиевые предметы, например, банки.
Алюминиевые банки
Металлический алюминий безопасен, но его соединения могут оказывать токсическое действие на человека и животных (особенно хлорид, ацетат и сульфат алюминия).
Физические свойства алюминия
Алюминий — достаточно легкий металл серебристого цвета, который может образовывать сплавы с большинством металлов, особенно с медью, магнием и кремнием. Также он весьма пластичен, его без труда можно превратить в тонкую пластинку или же фольгу. Температура плавления алюминия = 660 °C, а температура кипения — 2470 °C.
Химические свойства алюминия
При комнатной температуре металл покрывается прочной пленкой оксида алюминия Al₂O₃, которая защищает его от коррозии.
С окислителями алюминий практически не реагирует из-за защищающей его оксидной пленки. Однако ее можно легко разрушить, чтобы металл проявил активные восстановительные свойства. Разрушить оксидную пленку алюминия можно раствором или расплавом щелочей, кислотами или же с помощью хлорида ртути.
Благодаря восстановительным свойствам алюминий нашел применение в промышленности — для получения других металлов. Этот процесс называется алюмотермией. Такая особенность алюминия заключается во взаимодействии с оксидами других металлов.
Алюмотермическая реакция с участием оксида железа (III) [Wikimedia]
Например, рассмотрим реакцию с оксидом хрома:
Cr₂O₃ + Al = Al₂O₃ + Cr.
Алюминий хорошо вступает в реакцию с простыми веществами. Например, с галогенами (за исключением фтора) алюминий может образовать иодид, хлорид, или бромид алюминия:
2Al + 3Cl₂ → 2AlCl₃
С другими неметаллами, такими как фтор, сера, азот, углерод и т.д. алюминий может реагировать только при нагревании.
Также серебристый металл вступает в реакцию и со сложными химическими веществами.Например, с щелочами он образует алюминаты, то есть комплексные соединения, которые активно используются в бумажной и текстильной промышленности. Причем в реакцию вступает как гидроксид алюминия
Al(ОН)₃ + NaOH = Na[Al(OH)₄]),
так и металлический алюминий или же оксид алюминия:
2Al + 2NaOH + 6Н₂О = 2Na[Al(OH)₄] + ЗН₂.
Al₂O₃ + 2NaOH + 3H₂O = 2Na[Al(OH)₄]
С агрессивными кислотами (например, с серной и соляной) алюминий реагирует довольно спокойно, без воспламенения.
Если опустить кусочек металла в соляную кислоту, то пойдет медленная реакция — сначала будет растворяться оксидная пленка — но затем она ускорится. Алюминий растворяется в соляной кислоте с выделением водорода. В результате реакции получается хлорид алюминия:
Al₂O₃ + 6HCl = 2AlCl₃ + 3H₂O
2Al + 6HCl → 2AlCl₃ + 3H₂.
Хлорид алюминия [Wikimedia]
Здесь вы найдете интересные опыты на изучение химических свойств металлов.
Реакция алюминия с водой
Если опустить алюминиевую стружку в обычную воду, ничего не произойдет, потому что алюминий защищен оксидной пленкой, которая не дает этому металлу вступить в реакцию.
Только сняв защитную пленку хлоридом ртути, можно получить результат. Для этого металл нужно вымачивать в растворе хлорида ртути на протяжении двух минут, а затем хорошо его промыть. В результате получится амальгама, сплав ртути и алюминия:
3HgCI₂ + 2Al = 2AlCI₃ + 3Hg
Причем она не удерживается на поверхности металла. Теперь, опустив очищенный металл в воду, можно наблюдать медленную реакцию, которая сопровождается выделением водорода и образованием гидроксида алюминия:
2Al + 6H₂O = 2Al(OH)₃ + 3H₂.
Источник: https://melscience.com/ru/articles/alyuminij-i-ego-reakciya-s-vodoj/
Виды морской коррозии
В морской воде протекает 2 вида коррозии.
Наиболее распространенными среди них считаются следующие:
- Контактная. Проявляется из-за контакта жидкости и металла. Причиной становится хорошая электропроводность. Если рядом в воде находится несколько металлических изделий, металл становится по отношению к стали катодом.
- Электрокоррозия. Появляется, потому что в воде находятся блуждающие токи. Иногда проблемы оказываются связанными и с самими морскими судами, состоянием проложенной на них электросети.
Коррозия металла в морской воде способна за короткое время вывести из строя даже крупную металлоконструкцию. Как результат – она теряет прочность и обрушиться.
Это всегда риск появления человеческих жертв и больших убытков.
К 2022 году разработано множество средств, позволяющих или обеспечить защиту от агрессивной среды или замедлить протекание процесса. Их качество доказано на практике – удается получить заметный результат.
Рассмотрим вопросы защиты от морской коррозии более подробно.
Способы борьбы с коррозией алюминия
Алюминий – широко распространенный в промышленности и быту металл. Окисление алюминия на воздухе не происходит. Его инертность обусловлена тонкой оксидной пленкой, защищающей его. Однако под влиянием определенных факторов из окружающей среды этот метал все же подвергается разрушительным процессам, и коррозия алюминия — не такое уж и редкое явление.
Виды коррозии
Окисляется алюминий в атмосфере быстро, но на небольшую глубину. Этому препятствует защитная окисная пленка. Окисление ускоряется выше температуры плавления алюминия. Если нарушается целостность оксидной пленки, алюминий начинает корродировать. Причинами истончения его защитного слоя могут стать различные факторы, начиная с воздействия кислот, щелочей и заканчивая механическим повреждением.
Коррозия алюминия – саморазрушение металла под воздействием окружающей среды. По механизму протекания выделяют:
- Химическую коррозию – происходит в газовой среде без участия воды.
- Электрохимическую коррозию – протекает во влажных средах.
- Газовое разрушение – но сопровождает нагрев и горячую обработку алюминия. В результате взаимодействия кислорода с металлами возникает плотная окисная пленка. Вот почему алюминий не ржавеет, как и все цветные металлы.
На видео: электрохимическая коррозия металлов и способы защиты.
Причины коррозии алюминия
Коррозионная стойкость алюминия зависит от нескольких факторов:
- чистоты – наличия примесей в металле;
- воздействующей среды – алюминий может одинаково подвергаться разрушению и на чистом сельском воздухе и в промышленно загрязненных районах;
- температуры.
Во многих случаях малоконцентрированные кислоты могут растворить алюминий. От возникновения коррозии не защищает естественная окисная пленка.
Мощные разрушители – фтор, калий, натрий. Алюминий и его сплавы корродируют при воздействии химических соединений брома и хлора, растворов извести и цемента.
Коррозия алюминия и его сплавов происходит в воде, воздухе, оксидах углерода и серы, растворах солей. Морская вода приводит к ускоренному разрушению. Алюминий считается активным металлом, но при этом отличается хорошими коррозионными свойствами.
Выделяют два основных фактора, которые влияют на интенсивность коррозийного процесса:
- степень агрессивности воздействующей окружающей среды – влажность, загрязненность, задымленность;
- химическая структура.
Защита алюминия от коррозии (видео)
Алюминий – широко распространенный в промышленности и быту металл. Окисление алюминия на воздухе не происходит. Его инертность обусловлена тонкой оксидной пленкой, защищающей его. Однако под влиянием определенных факторов из окружающей среды этот метал все же подвергается разрушительным процессам, и коррозия алюминия — не такое уж и редкое явление.
Коррозионная стойкость алюминия
Окись алюминия создает защитный слой, толщина которого составляет 20—100Å, который химически инертен. Чистый алюминий, с поверхностью, очищенной от защитной пленки, реагирует с водой, выделяя при этом водород и создавая оксидную пленку на поверхности.
Таким образом, при контакте с окислителями, поверхность алюминия пассивируется. По сути, кислород, содержащийся в воздухе или растворенный в воде, повышает коррозионную стойкость алюминия, которая, в свою очередь, в значительной степени зависит от содержания примесей других металлов.
Известно, что при контакте двух металлов, в среде электролита, образуется гальваническая пара, где анодом становится более активный металл, а катодом — менее активный. В результате электрохимической реакции происходит разрушение структуры анода. Большая часть примесей (железо, свинец, медь и т.д.
) играют по отношению к алюминию роль катода, способствуя его разрушению. По этой причине чистый алюминий имеет более высокую стойкость к коррозии, чем технический, который, в свою очередь, более стоек к коррозии, чем сплавы алюминия с другими металлами.
Так же стойкость алюминия к коррозии зависит от характеристик внешней среды и от реакций, вызываемых этой средой.
Рис.2. Механизм образования оксидной пленки на алюминии
Заключение
Алюминий имеет высокую стойкость к коррозии, однако, при контакте с другими металлами или при воздействии электрического тока подвержен коррозии. Мерами по защите алюминиевых светопрозрачных конструкций от коррозии являются нанесение порошкового покрытия или анодирование, а так же использование нержавеющего или оцинкованного крепежа и элементов конструкции.
: Молоко с цементом для защиты бочек от ржавчины: изучаем суть
Оксидирование алюминия
Оксидирование алюминия протекает при постоянном токе под напряжением 250 В. Наращивание защитной пленки происходит при комнатной температуре с водяным охлаждением. Не требуется импульсного источника. Пленки получаются плотными и прочными в течение 45-60 минут.
На плотность и цвет оксидного покрытия влияет температура электролита:
- пониженная температура образует плотную пленку яркого цвета;
- повышенная – формирует рыхлую пленку, требующую дальнейшей окраски.
Образовать защиту алюминия от коррозии можно электрохимической реакцией. Процесс разделен на несколько этапов:
1. На стадии подготовки алюминиевое изделие обезжиривают, погружая его в раствор щавелевой кислоты.
2. После промывания водой опускают в щелочной раствор, чтобы удалить неравномерно образовавшийся оксидный слой.
3. Для дополнительной окраски алюминиевые изделия погружают в соответствующие растворы солей. Чтобы заполнить образовавшиеся поры, металлический материал обрабатывают паром.
4. Затем изделие подвергают сушке. Анодное оксидирование может проводиться с применением переменного тока.
Для защиты от коррозии применяют химическое оксидирование – менее затратное, не требующее специального электрического оборудования и квалификации исполнителей. Используется несложный химический состав.
В процессе алюминирования полученная оксидная пленка толщиной в 3 мкм имеет салатный цвет, обладает высокими электроизоляционными свойствами, не пориста, не окрашивается.
Коррозия алюминия возникает вследствие находящихся рядом металлов, которые окислились. Предотвращению этот процесса способствует изоляция. Это могут быть прокладки из резины, битума, паронита. При покрытии ржавчиной применяются лак и другие изолирующие материалы. Других способов избавиться от этой проблемы пока нет.
Основные виды коррозии алюминия
Алюминий и, в разной степени, его сплавы обладают высокой стойкостью к коррозии даже без какого-либо специального защитного покрытия.
Естественное оксидное покрытие
Естественная поверхность алюминия, которая возникает в ходе изготовления алюминиевого изделия, например, прессованием, прокаткой или литьем, имеет высокое сопротивление коррозии в большинстве типов окружающей среды. Это происходит потому, что свежая поверхность алюминия спонтанно и мгновенно образует тонкий, но очень эффективный оксидный слой, который предотвращает дальнейшее окисление металла.
Эта оксидная пленка является непроницаемой и, в отличие от оксидных пленок других металлов, например, железа, очень прочно «прикрепляется» к основному металлу. При каком-либо механическом повреждении эта пленка мгновенно восстанавливается, залечивается.
Естественный оксидный слой и является главной причиной хорошего сопротивления алюминия к коррозии. Это покрытие является стойким в средах с кислотностью – водородным показателем рН – от 4 до 9.
Три главных вида коррозии алюминия
Наиболее частыми видами коррозии алюминия являются:
- гальваническая (контактная) коррозия;
- язвенная (точечная) коррозия;
- щелевая коррозия.
Коррозия под напряжением, которая ведет к образованию трещин, является более специфическим видом коррозии. Она случается в основном в высокопрочных алюминиевых сплавах, например, сплавах AlZnMg, когда они подвергаются длительным растягивающим напряжениям в присутствии коррозионной среды. Этот тип коррозии обычно не происходит в сплавах серии 6ххх, то есть сплавах AlMgSi.
Гальваническая коррозия алюминия
Гальваническая коррозия может случаться тогда, когда два различных металла находятся в непосредственном контакте и между ними образовался электролитический мост. Менее благородный металл в этой комбинации становится анодом и корродирует. Более благородный металл становиться катодом и находится под защитой от коррозии.
В большинстве комбинаций с другими металлами алюминий является менее благородным металлом. Поэтому алюминий подвержен более высокому риску гальванической коррозии, чем другие строительные материалы. Однако, этот риск меньше, чем это обычно считается.
Необходимые условия: контакт и влага
Гальваническая коррозия алюминия происходит только тогда, когда одновременно:
- есть контакт с более благородным металлом (или другим электрическим проводником с более высоким химическим потенциалом, чем у алюминия, например, графитом;
- между двумя металлами находится электролит с хорошей проводимостью, чаще всего, вода с растворенными солями.
Гальваническая коррозия не происходит в сухой воздушной атмосфере, например, внутри нормального жилого помещения. Нет большого риска гальванической коррозии и чистой сельской атмосфере. Вместе с тем, риск гальванической коррозии необходимо всегда принимать в расчет в атмосферах с высоким содержанием хлоридов, например, в районах вблизи морей и океанов.
Алюминий и оцинкованная сталь
Могут быть проблемы с гальванической коррозией и в паре алюминия с оцинкованной сталью. Цинковое покрытие оцинкованной стали будет сначала защищать алюминий от коррозии.
Однако, эта защита снижается, когда поверхность стали начинает обнажаться по мере расходования цинка. Горячее цинкование стали дает большую толщину цинкового покрытия, чем электрохимическое цинкование и обеспечивает более длительную защиту алюминия.
Поэтому в агрессивной атмосфере в контакте с алюминием применяют только оцинкованную сталь горячего цинкования.
Электрическая изоляция
Там, где различные металлы применяются в контакте, гальванической коррозии можно избежать путем электрической изоляции одного металла от другого. Пример такого решения для болтового соединения между алюминиевым и стальным листом приведен на рисунке 1.
Между головкой болта и поверхностью алюминия может возникнуть электролит, но электроизолирующая шайба не даст возможности протекать гальваническому электрическому току и коррозии не произойдет.
С другой стороны в контакте алюминиевого и стального листа отсутствует возможность попадания влаги, электролит не образуется и коррозия не происходит.
Rus-npf
1. Введение Как правило, алюминиевые сплавы обладают хорошими антикоррозионными свойствами в следующих средах: атмосфера, пресная вода, морская вода, большинство типов почвы, продуктов питания и множество химикатов. Термин «хорошая коррозионная стойкость» означает, что в большинстве случаев можно использовать алюминий без защитных покрытий и при этом срок службы будет долгим. В зависимости от агрессивности среды, а также назначения продукта, расчетного срока эксплуатации и требований к техническому обслуживанию, могут быть предприняты меры по противодействию или снижению степени коррозионного воздействия. Могут применяться несколько способов защиты. В этой лекции рассматриваются только те меры, которые относятся к незащищенным алюминиевым изделиям и компонентам. Защитные обработки поверхности, такие как предварительная обработка, покраска и анодирование.
2. Выбор коррозиестойких сплавов
Добавка легирующих элементов в алюминий влияет на характер коррозии, и важно выбрать наиболее пригодный сплав для каждой среды. Наиболее часто в качестве легирующих добавок в алюминиевых сплавах используют: медь, магний, марганец, кремний и цинк, а в качестве примесей в технически чистый алюминий – железо и кремний.
2.1. Кованые алюминиевые сплавы
Чистый алюминий (>99,9 % Al)
Сверхчистый алюминий (>99,9% Al) проявляет наилучшие для алюминия антикоррозионные свойства. Эти показатели резко снижаются с введением примесей, особенно меди и железа.
Al-Mn
Сплавы Al-Mn имеют хорошие антикоррозионные свойства и применяются вне помещений без защиты.
Al-Mg
Обычно, сплавы Al-Mg имеют наилучшие антикоррозионные свойства из всех сплавов алюминия. При содержании магний свыше 4%, технология изготовления оказывает заметное влияние на долговременные характеристики в коррозионных средах, даже при нормальных температурах. При длительном воздействии температуры свыше 60о С сплавы с большим содержанием магния становятся уязвимы к растрескиванию под напряжением и отслаиванию.
Al-Cu
Сплавы, содержащие существенное количество меди (> 0,25%) обладают меньшими антикоррозионными свойствами и потому не должны использоваться в агрессивных морских или промышленных средах без защитных покрытий. В прошлом, наиболее распространенной ошибкой было использование сплавов Al-Cu в коррозионных средах без соответствующих защитных мер.
Al-Zn-Mg-Cu
Сплавы, содержащие Zn, Mg и Cu обладают сходными коррозионными качествами, что и семейство сплавов Al-Cu и поэтому требуют защитных мер в коррозионных средах.
Al-Zn-Mg
Для этого семейства сплавов технология изготовления, особенно термическая обработка и состав сплава имеют решающее значение для коррозионного поведения. Сплавы из Al-Zn-Mg могут быть чувствительны к растрескиванию от коррозии под напряжением и отслаиванию.
2.2. Литейные алюминиевые сплавы
Коррозия в литых заготовках из алюминия обычно меньше чем в листовых изделиях, поскольку обычно, профиль толще и способен выдержать более суровую поверхностную коррозию. Литейные сплавы из Al-Mg имеют хорошие антикоррозионные свойства и могут применяться в морских средах. Считается, что Al-Si обладает хорошей коррозионной стойкостью в атмосфере и воде. Сплавы из Al-Cu и Al-Si-Cu требуют защиты поверхности в коррозионных средах. Поведение любого сплава зависит от среды, которую он должен выдержать; В качестве примера приведенная ниже таблица показывает поведение различных сплавов в кислотах и щелочах. Чем ниже показатель, тем лучше сопротивляемость к коррозии.
3. Усовершенствование конструкции оборудования
Поскольку поведение коррозии в металлах зависит от физических и химических условий среды (например, температуры, примесей, изменение концентрации и т.д.) а также от химического состава, конструкция может значительно влиять на характер и скорость коррозии. Наиболее распространенные конструкционные отказы при обслуживании алюминиевых изделий включают в себя электрохимическую, щелевую и коррозию под напряжением. В следующих параграфах даются рекомендации по предотвращению или, по крайней мере, снижению воздействия от этих видов коррозии:
3.1. Предотвращение электрохимической коррозии
Предлагаются следующие «правила» для уменьшения электрохимической коррозии: Выбор комбинаций металлов как можно ближе стоящих друг к другу в ряде электродных потенциалов для рассматриваемой среды. Использовать катодные крепления. Избегать комбинаций с неблагоприятным (малым) отношением площади анода к катоду. Обеспечить полную электрическую изоляцию двух соединенных металлов. Это можно сделать, если использовать изолирующую прокладку, втулки (трубки) и др. Если применяется краска, всегда красьте катод. Если покрасить только анод, любая царапина привела бы к неблагоприятному отношению площади анода к катоду, и к коррозии в месте царапины. Увеличение толщины анодного материала. В качестве альтернативы можно установить небольшие съемные толстые профили из анодного металла в месте соединения. По возможности, размещать разнородный металлический контакт вдали от коррозионной среды. По возможности, избегать резьбовых соединений разнородных пар, т.к. резьба может разрушиться. Желательно соединять припоем или сваркой. Если возможно, использовать ингибиторы коррозии (например, в системах циркуляции). В тех случаях, когда металлы должны оставаться в электрическом контакте через внешнюю цепь, проектировать оборудование таким образом, чтобы металлы располагались как можно дальше друг от друга, тем самым, увеличивая электрическое сопротивление через жидкость (электролит). По необходимости и возможности использовать катодную защиту с использованием цинкового или магниевого протекторного анода. Для большинства агрессивных сред, только цинк, кадмий и магний могут контактировать с алюминием не вызывая электрохимической коррозии.
3.2. Предупреждение коррозии вследствие отложений
Следующие меры помогут снизить данный вид коррозии на алюминии
1. Перепроектировать для того, чтобы избежать отложения более благородного металла, например, используя дренажную систему
2. Применение Алькледа
3. Использование ингибиторов
4. Покраска металлической основы
5. Многократная очистка для удаления осажденного благородного металла
3.3. Предупреждение щелевой коррозии
Для проекта из алюминиевых конструкций подверженных воздействию морской атмосферы в течение продолжительного времени должны предприниматься меры по предупреждению щелевой коррозии.
Следующие меры помогут снизить щелевую коррозию в алюминиевых конструкциях:
1. Покрывать прилегающие поверхности перед сборкой ингибирующей лакокрасочной композицией
2. Заполнять щель замазкой (мастикой) или эластичным прокладочным материалом для предотвращения доступа влаги.
3.4. Предупреждение коррозии под напряжением
Для проекта из алюминиевых конструкций находящихся под постоянным напряжением (нагрузкой), следует предпринять ряд мер, чтобы минимизировать коррозию под напряжением.
Следующие меры помогут снизить эффект воздействия от такого вида коррозии в алюминиевых конструкциях:
1. Убедитесь, что выбран адекватный профиль, который не будет перегружен. Особое внимание следует уделять остаточным или монтажным напряжениям, действующим в коротком поперечном направлении.
2. Хорошая лакокрасочная композиция, включающая противокоррозионную грунтовку придаст дополнительную защиту от коррозии под напряжением. Однако, необходимо осознавать, что лакокрасочные покрытия не являются полностью непроницаемыми для влаги и потому не следует ожидать от них хорошей защиты особо чувствительных к коррозии сплавов.
3. Металлизация распылением с некоторыми алюминиевыми сплавами вносит заметный вклад в коррозионную защиту, которую следует в дальнейшем усилить при помощи краски.
4. Методы обработки поверхности, такие как дробеструйная обработка или шлифовка для получения остаточного напряжения сжатия, при правильном применении позволяют эффективно снизить масштабы коррозионного растрескивания под напряжением.
5. Приложенное напряжение. Постоянные приложенные напряжения растяжения на поверхности не должны превышать следующих пределов: в продольном направлении 50% предела текучести; по длинному поперечному направлению между 35 и 50% предела текучести; по кратчайшему поперченному направлению: как можно меньше и желательно не больше 15% предела текучести.
3.5. Сплавы с хорошей сопротивляемостью к коррозии под напряжением
Ряд систем из высокопрочных алюминиевых сплавов восприимчивы к термическим обработкам (старение), при которых достигаются металлургические состояния с гораздо большей сопротивляемостью к коррозии под напряжением без потерь механический свойств (сплавы Т76, Т73). Все эти рекомендации имеют общий характер и в каждом конкретном случае необходимо подробное изучение.
4. Изменение среды
Иногда можно снизить или даже свести на нет агрессивность среды, тем или иным способом изменяя последнюю. В некоторых химических веществах, например феноле, при добавлении небольшого количества воды (например, 0,3%) предотвратит сильную коррозию, которая бы возникла бы при отсутствии воды. В других веществах, таких как жидкий диоксид серы, вода способствует коррозии алюминия. Обычно, движение или турбулентность, не чрезмерная, иногда предотвращает точечную коррозию, которая возникла бы в противном случае. Приведение показателя рН до безопасного диапазона (от 4.5 до 8.5) предотвращает или снижает коррозию. Деаэрация воды значительно снижает тенденцию образования коррозионных язв в алюминии. Повышение температуры, обычно, может усилить скорость общей (равномерной) коррозии, но при этом благоприятно влияет на снижение скорости точечной коррозии. Очевидно, что эти воздействия являются специфичными для особых (отдельных) условий, и по этому вопросу можно сказать немногим больше, чем сказано выше.
4.1. Ингибиторы коррозии
Ингибитор это вещество, при добавлении которого (обычно в небольших количествах) в агрессивную жидкость или химикат снижается или предотвращается коррозия металла, возникающая в обратном случае. Ингибиторы могут воздействовать на анодную коррозию, в этом случае их принято называть «анодными ингибиторами», либо могут воздействовать на катодную коррозию, тогда их называю «катодными ингибиторами». Анодные ингибиторы могут представлять опасность, если их не добавить в достаточном количестве, т.к. в то время как они уменьшают эффективную площадь анода, воздействие на оставшиеся участки будет более суровым, чем в отсутствие ингибитора. Катодные ингибиторы более безопасные, поскольку частичное уменьшение эффективной площади катода снижает коррозию на аноде. Однако, обычно они менее эффективны по сравнению с анодными ингибиторами. Хромат (в виде хромата калия или калия или дихромата) наиболее часто используется в качестве ингибитора с алюминием и принадлежит к анодным ингибиторам. Для предотвращения точечной коррозии алюминия в агрессивной воде, полезно добавить 500 ppm. (промиль) хромата натрия или дихромата с рН 8.5 Фосфат, силикат, нитрат, нитрит, бензоат, растворимое масло и другие вещества также рекомендуются в отдельности или в сочетании для снижения воздействия коррозии алюминия со стороны агрессивных жидкостей. Ингибирование воды обычно целесообразно только в рециркуляционных, замкнутых системах. В смешанных системах включающих, например, алюминий и медь важно спроектировать хорошую ингибиторную систему и поддерживать показатель рН выше 8.0-8.5, чтобы не допустить растворение меди и ее последующее отложение на поверхности алюминия. Сложность ингибирования заключается в том, что обычному инженеру трудно добиться достаточной водоподготовки без помощи специалиста. Часто, необходимы лабораторные тесты на месте, чтобы достигнуть наилучших параметров.
5. Катодная защита
Теория катодной защиты металла проложенного в грунте простая. Постоянный электрический ток (вызываемый протекторными анодами или подаваемый ток) подается на защищаемый металл. Этот ток поляризует локальные катодные участки до потенциала локального анода и создает поверхность с равномерным потенциалом. Таким образом, потенциал гальванической ячейки становится равным нулю и точечной коррозии не возникает. Ток может производиться ректификатором с металлическим или графитовым электродом или протекторными гальваническими анодами из магния или цинка. Для того чтобы уменьшить требуемый ток, защищаемый металл иногда покрывают краской, защитной пленкой или другим оберточным материалом. В индустрии стальных трубопроводов метод протекторной защиты хорошо налажен и продемонстрировал достаточную эффективность. Опыт проложенного в земле алюминия ограничивается единичными экспериментами и ограниченным числом рабочих линий.
Протекторные аноды
Алюминий может быть катодно защищен путем соединения его с цинком или магнием, используемым как протекторный анод. В случаем с алюминием, возможно механизм защиты состоит из поляризации катодных примесей в металле до коррозионного потенциала пассивного алюминия, препятствующего неблагоприятному воздействию таких примесей. Цинк может применяться как протекторный анод по отношению к алюминию в нейтральной или чуть кислотной среде, несмотря на тот факт, что алюминий более активный, чем цинк в ряде электродных потенциалов. В щелочной среде алюминий теряет свою пассивность и становится анодом по отношению к цинку. Магний обычно используют для защиты алюминия в ряде случаев. Установка анодов из магния позволят остановить коррозию даже в трубопроводах, проложенных в земле с накопленными продуктами коррозии. В некоторых случаях излишняя защита может привести к образованию катодной коррозии алюминия. Потенциал создаваемый между анодами магния и алюминия обычно не превышает 1.20 вольт (Cu/SO4) и, обычно, благодаря щелочной структуре, катодной коррозии не происходит.
5.1. Подаваемый ток
Катодная защита с помощью катодного тока требует наличия источника постоянного тока и вспомогательного электрода, как показано на рисунке 5104.04.01. Источник постоянного тока соединен положительной клеммой к вспомогательному электроду, а отрицательной к защищаемой конструкции. Ток течет от электрода через электролит к конструкции. Общепринято, что защита алюминия обеспечивается в том случае, если потенциал поверхности алюминия проложенного в земле поддерживается в диапазоне от -0.85 до -1.10 вольт (Cu/SO4) и существенной катодной коррозии не возникает пока не превышено значение -1.20 вольт. Химический состав почвы может влиять на безопасный верхний потенциал, который в ряде случаев может значительно превышать -1.20 вольт. Требуемая плотность тока зависит от среды, но, обычно, плотность подаваемого тока должна всегда превышать эквивалент плотности тока, расчетной или измеряемой скорости коррозии (в водопроводной воде модно взять за расчет приблизительно 20 мА/м2, в почве в среднем 5 мА/м2 ). Если используются защитные покрытия алюминия, плотность тока может быть меньше и для защиты 20 км трубы понадобиться лишь 90-240 мА.
5.2. Сплавы Альклед
Альклед это двухслойное изделие, состоящее из тонкого слоя одного сплава, полностью соединенного с другим, более толстым основным сплавом. Оболочный сплав исполняет роль протекторного анода для защиты основного сплава. Группа сплавов Al-Zn обычно применяется в качестве оболочных материалов для защитных целей, однако в ряде случаев используется чистый алюминий. Защитный механизм оболочки основан на протекторной защите. Когда язва достигает основного материала, оболочка коррозирует в первую очередь, в то время как основной слой остается нетронутым. Оболочка (плакирование) дает реальную возможность продлить срок службы алюминиевых трубопроводов, по которым доставляется продукт, вызывающий точечную коррозию металла. Принято, что оболочка на каждой стороне листа составляет 5% общей толщины листа.
Практические вопросы
Как минимизировать точечную коррозию алюминия в агрессивной воде?
Здесь необходимо рассмотреть четыре возможные превентивные меры:
1. Использование сплава Альклед
Применять 3003 или 65S покрытый 72S. Это не предотвратит точечную коррозию, но существенно задержит образование сквозных язв.
2. Увеличение толщины стенки
Опираясь на опыт эксплуатации больших водяных цистерн можно предположить, что при толщине стенки 6-7мм сквозная коррозия не возникает достаточно долгое время (50-100 лет), даже в случае образования точечной коррозии.
3. Применение ингибиторов
Использование ингибиторов для предотвращения точечной коррозии оправдано только для замкнутых систем циркуляции
4. Катодная защита
Катодная система защиты с подаваемым током предотвратит от точечной коррозии, или остановит ее развитие, и может использоваться как в цистернах, так и в кораблях. Невозможно применить катодную защиту для внутренней поверхности трубопроводов с небольшим диаметром.
Коррозия алюминия и методы его защиты
Алюминий и его сплавы отличаются отличной устойчивостью к разрушениям различного характера. Однако, несмотря на это — коррозия алюминия представляет собой не такое уж и редкое явление. Различные формы коррозии представляют собой основную причину порчи этих материалов. Для борьбы с разрушительными процессами необходимо обязательно понимать факторы, которые являются причиной их появления.
Коррозия алюминия представляет собой реакцию, которая имеет место между металлом и окружающей средой. Этот процесс может иметь как естественное, так и химическое происхождение. Самой распространенной формой разрушения металла можно назвать появление на его поверхности процессов ржавления.
Особенностью всех видов металлов можно назвать их свойство вступать в реакцию с водой и окружающей средой. Отличием для каждого вида металла считается только интенсивность данного процесса. К примеру, у благородных металлов типа золота скорость такой реакции не будет слишком быстрой, а вот железо, в том числе и алюминий, будут реагировать на воздействия такого характера достаточно быстро.
Можно выделить два фактора, которые оказывают непосредственное влияние на интенсивность протекания процесса коррозии. Одним из них можно назвать степень агрессивности окружающей среды, а вторым металлургическую или химическую структуру. Атмосфере, которая нас окружает, всегда характерен определенный уровень влажности. Кроме того, ей характерен определенный уровень загрязнений и отходов.
Если учесть, что свойства атмосферы часто определяются регионом и степенью индустриализации, на сегодняшний день можно выделить:
- сельская местность (малая степень загрязнений и средний уровень влажности);
- приморские области (средняя степень загрязнений и высокий уровень влажности);
- городская местность (средний уровень влажности и средний уровень продуктов распадов жидкого топлива, серы и окислов углерода);
- промышленные и индустриальные зоны (большое количество серы, окислов углеродов и кислот, а также средний уровень влажности)
Для большинства случаев, кислоты неорганического типа, даже при низкой концентрации смогут растворить алюминий. И даже натуральная пленка оксида алюминия не сможет стать достаточной защитой от возникновения коррозийных процессов.
Самыми мощными растворителями можно назвать фтор, калий и натрий. Кроме того, алюминию характерна довольно низкая сопротивляемость к соединениям хлора и брома. Весьма агрессивны к различным сплавам алюминиевых металлов, являются известковые и цементные растворы.
Можно выделить несколько разновидностей проявления коррозии алюминия и его сплавов:
- Поверхностная. Данный тип разрушения встречается чаще всего и является наименее вредоносным. Его легче всего заметить на поверхности. Это дает возможность своевременно использовать предохранительные средства. Поверхностные разрушения очень часто встречаются на анодированных профилях для строительства.
- Локальная. Такие разрушения проявляются в виде форм, углублений и пятен. Такой тип коррозии бывает поверхностного и междукристаллического типа. Разрушения такого характера являются особенно опасными, по причине того, что их достаточно сложно обнаружить. Такая коррозия очень часто разрушает именно труднодоступные части конструкций и узлов.
- Нитеподобная или филигранная. Этот вид разрушения алюминия часто появляется под покрытиями органического типа, а также на граничных поверхностях обработки. Нитеподобная коррозия появляется в ослабленных местах повреждения органического покрытия или краях отверстий;
Довольно часто, естественных антикоррозийных способностей алюминия и его сплавов для защиты от разрушений бывает недостаточно. А длительный период эксплуатации изделий из этих металлов, в обязательном порядке потребует использования дополнительных методов защиты. К самым частым методам протекции металлов от коррозии можно отнести:
- анодирование окисление (исследования немецких специалистов показывают, что данный вид защиты используется на 15% от общего количества производства строительных профилей в мире);
- покрытие поверхности металлов порошковыми составами;
- защита от контакта с другими металлами
Анодирование
Анодированное покрытие представляет собой покрытие, которое создает на поверхности алюминия прочную пленку из оксида алюминия, которая не поддается воздействию агрессивных сред. Такая обработка позволяет создать на поверхности металла такой слой пленки, который просто не оставляет алюминию возможности контактировать с внешней средой и ограждает его от процессов окисления.
Особенности протекания процесса
Морская коррозия металлов протекает под воздействием множества внешних агрессивных факторов. Как мы уже отмечали, этот процесс относится к электромеханическим разновидностям процессов.
Его протекание напрямую связано с кислородной деполяризацией и дифузионно-кинетическим катодным контролем.
Проблем добавляет то, что сама вода постоянно двигается. Это связано не только с давлением, но и с тем, что суда постоянно находятся в движении с собственной скоростью.
В зависимости от условий, в которых находится металлоконструкция, меняется тип контроля:
- При сильной аэрации и в местах с сильным течением, частым волнением, кинетический контроль выходит на первый план.
- На участках где морская вода находится в неподвижном состоянии, преобладающим оказывается катодный контроль.
Если рассматривать процесс как катодно-анодную реакцию, мы увидим, что в качестве анода выступает металл, в то время как катодом становится оксидная пленка на его поверхности.
Морская коррозия становится заметной быстро. Она вызывает масштабное разрушение материала, на нем появляются язвы большой глубины, структура металла разрушается и становится хрупкой. Материал уже переносит прежнего нагрузок.
Также не стоит сбрасывать со счетов атмосферную коррозию в морских районах. Она связана с особым составом воздуха, воздействием других особых условий среды.
Коррозия алюминия
Коррозия алюминия – разрушение металла под влиянием окружающей среды.
Для реакции Al3+ +3e → Al стандартный электродный потенциал алюминия составляет -1,66 В.
Температура плавления алюминия — 660 °C.
Плотность алюминия — 2,6989 г/см3 (при нормальных условиях).
Алюминий, хоть и является активным металлом, отличается достаточно хорошими коррозионными свойствами. Это можно объяснить способностью пассивироваться во многих агрессивных средах.
Коррозионная стойкость алюминия зависит от многих факторов: чистоты металла, коррозионной среды, концентрации агрессивных примесей в среде, температуры и т.д. Сильное влияние оказывает рН растворов. Оксид алюминия на поверхности металла образуется только в интервале рН от 3 до 9!
Очень сильно влияет на коррозионную стойкость Al его чистота. Для изготовления химических агрегатов, оборудования используют только металл высокой чистоты (без примесей), например алюминий марки АВ1 и АВ2.
Коррозия алюминия не наблюдается только в тех средах, где на поверхности металла образуется защитная оксидная пленка.
При нагревании алюминий может реагировать с некоторыми неметаллами:
2Al + N2 → 2AlN – взаимодействие алюминия и азота с образованием нитрида алюминия;
4Al + 3С → Al4С3 – реакция взаимодействия алюминия с углеродом с образованием карбида алюминия;
2Al + 3S → Al2S3 – взаимодействие алюминия и серы с образованием сульфида алюминия.
Коррозия алюминия на воздухе (атмосферная коррозия алюминия)
Алюминий при взаимодействии с воздухом переходит в пассивное состояние. При соприкосновении чистого металла с воздухом на поверхности алюминия мгновенно появляется тонкая защитная пленка оксида алюминия. Далее рост пленки замедляется. Формула оксида алюминия – Al2O3 либо Al2O3•H2O.
Реакция взаимодействия алюминия с кислородом:
4Al + 3O2 → 2Al2O3.
Толщина этой оксидной пленки составляет от 5 до 100 нм (в зависимости от условий эксплуатации). Оксид алюминия обладает хорошим сцеплением с поверхностью, удовлетворяет условию сплошности оксидных пленок. При хранении на складе, толщина оксида алюминия на поверхности металла составляет около 0,01 – 0,02 мкм. При взаимодействии с сухим кислородом – 0,02 – 0,04 мкм. При термической обработке алюминия толщина оксидной пленки может достигать 0,1 мкм.
Алюминий достаточно стоек как на чистом сельском воздухе, так и находясь в промышленной атмосфере (содержащей пары серы, сероводород, газообразный аммиак, сухой хлороводород и т.п.). Т.к. на коррозию алюминия в газовых средах не оказывают никакого влияния сернистые соединения – его применяют для изготовления установок переработки сернистой нефти, аппаратов вулканизации каучука.
Коррозия алюминия в воде
Коррозия алюминия почти не наблюдается при взаимодействии с чистой пресной, дистиллированной водой. Повышение температуры до 180 °С особого воздействия не оказывает. Горячий водяной пар на коррозию алюминия влияния также не оказывает. Если в воду, даже при комнатной температуре, добавить немного щелочи – скорость коррозии алюминия в такой среде немного увеличится.
Взаимодействие чистого алюминия (не покрытого оксидной пленкой) с водой можно описать при помощи уравнения реакции:
2Al + 6H2O = 2Al(OH)3 + 3H2↑.
При взаимодействии с морской водой чистый алюминий начинает корродировать, т.к. чувствителен к растворенным солям. Для эксплуатации алюминия в морской воде в его состав вводят небольшое количество магния и кремния. Коррозионная стойкость алюминия и его сплавов, при воздействии морской воды, значительно снижается, если в состав метала будет входить медь.
Коррозия алюминия в кислотах
С повышением чистоты алюминия его стойкость в кислотах увеличивается.
Коррозия алюминия в серной кислоте
Для алюминия и его сплавов очень опасна серная кислота (обладает окислительными свойствами) средних концентраций. Реакция с разбавленной серной кислотой описывается уравнением:
2Al + 3H2SO4(разб) → Al2(SO4)3 + 3H2↑.
Концентрированная холодная серная кислота не оказывает никакого влияния. А при нагревании алюминий корродирует:
2Al + 6H2SO4(конц) → Al2(SO4)3 + 3SO2↑ + 6H2O.
При этом образуется растворимая соль – сульфат алюминия.
Al стоек в олеуме (дымящая серная кислота) при температурах до 200 °С. Благодаря этому его используют для производства хлорсульфоновой кислоты (HSO3Cl) и олеума.
Коррозия алюминия в соляной кислоте
В соляной кислоте алюминий или его сплавы быстро растворяются (особенно при повышении температуры). Уравнение коррозии:
2Al + 6HCl → 2AlCl3 + 3H2↑.
Аналогично действуют растворы бромистоводородной (HBr), плавиковой (HF) кислот.
Коррозия алюминия в азотной кислоте
Концентрированный раствор азотной кислоты отличается высокими окислительными свойствами. Алюминий в азотной кислоте при нормальной температуре исключительно стоек (стойкость выше, чем у нержавеющей стали 12Х18Н9). Его даже используют для производства концентрированной азотной кислоты методом прямого синтеза
При нагревании коррозия алюминия в азотной кислоте проходит по реакции:
Al + 6HNO3(конц) → Al(NO3)3 + 3NO2↑ + 3H2O.
Коррозия алюминия в уксусной кислоте
Алюминий обладает достаточно высокой стойкостью к воздействию уксусной кислоты любых концентраций, но только если температура не превышает 65 °С. Его используют для производства формальдегида и уксусной к-ты. При более высоких температурах алюминий растворяется (исключение составляют концентрации кислоты 98 – 99,8%).
В бромовой, слабых растворах хромовой (до10%), фосфорной (до 1%) кислотах при комнатной температуре алюминий устойчив.
Слабое влияние на алюминий и его сплавы оказывают лимонная, масляная, яблочная, винная, пропионовая кислоты, вино, фруктовые соки.
Щавелевая, муравьиная, хлорорганические кислоты разрушают металл.
На коррозионную стойкость алюминия очень сильно влияет парообразная и капельножидкая ртуть. После недолгого контакта металл и его сплавы интенсивно корродируют, образуя амальгамы.
Ржавеет ли алюминий: свойства материала, причины коррозии и способы защиты
Алюминий является материалом, который люди часто используют в промышленности и для собственных нужд. Подобный металл отличается гибкостью, а также устойчивостью к внешним воздействиям. Он не токсичен и безопасен для здоровья человека. Серебряный цвет позволяет применять металл для различных целей. Это промышленность и бытовая сфера.
При работе в промышленности люди часто задаются вопросом, ржавеет ли алюминий. Всем известно, что если на листе появляется повреждение, то может развиться коррозия. Следует узнать, почему алюминий ржавеет иначе, чем другие сплавы. Необходимо выяснить причины, по которым он подвергается коррозии. Обо всем этом и не только — читайте в нашей сегодняшней статье.
Свойства
Кругом полымя! Значения слова не знаю, но чувствую — припекает
Давайте изучим характеристики алюминия. Описываемый металл плавится при температуре 659 градусов Цельсия. Плотность вещества составляет 2,69*103 кг/см3. Алюминий относят в группу активных металлов. Устойчивость к коррозионным процессам зависит от ряда факторов:
- Чистота сплава. Для производства различного оборудования берут металл, отличающейся своей чистотой. В нем не должно быть различных примесей. Широко распространен алюминий марки АИ1, а также АВ2.
- Среда, в которой находится алюминий.
- Какая концентрация примесей в окружающей алюминий среде.
- Температура.
- Большое влияние оказывает рН среды. Нужно знать, что оксид алюминия может образовываться, когда рН находится в интервале между 3 и 9. В той среде, где на поверхности листа алюминия сразу же появляется оксидная пленка, коррозионные процессы развиваться не будут.
- Взаимодействие с какой-либо кислотой или щелочью.
- Механическое давление. Например, трение или сильный удар, после чего появляется царапина на верхнем слое металла.
- Существуют промышленные районы. В них продукты распада топлива влияют на оксидную пленку и разрушают ее. Металл начинает портиться. Аналогичная ситуация происходит в мегаполисах, где продукты распада топлива будут взаимодействовать с серой, а также с оксидами углерода. Подобный процесс разрушает пленку на алюминии. После такого рода внешнего воздействия алюминий подвергается коррозии.
- Следует помнить, что хлор, фтор, а также бром и натрий могут растворить защитный слой металла.
- Если на металл попадают строительные смеси, то он начинает быстро портиться. В данном случае на алюминий неблагоприятно воздействует цемент.
- Ржавеет ли алюминий от воды? Если она попадает на лист, то металл может быть подвержен коррозионным процессам. Важно при этом уточнить, какая жидкость оказывает воздействие. Многие используют специальный сплав, который не подвержен коррозии от воды. Его называют дюралюминием. Уникальный сплав используют вместе с медью, а также с марганцем.
- Чтобы свойства алюминия, препятствующие коррозии, сохранялись, необходимо поддерживать кислотно-щелочной баланс. Диапазон должен составлять от шести до восьми единиц.
- Считается, что чистый металл, без примесей, лучше противостоит агрессивной среде. Учеными были проведены эксперименты. По результатам можно сказать, сплавы чистого алюминия (90%) подвержены коррозии больше, чем сплав, содержащий 99% этого вещества. У первого варианта коррозия наступает в 80 раз быстрее, чем у второго сплава.
- Чтобы в агрессивной среде металл дольше не терял свои свойства, его обрабатывают специальной краской. Можно использовать полимерный состав. После обработки появляется дополнительный защитный слой.
- Если добавить в сплав при производстве 3% марганца, то появится возможность избежать коррозии алюминия.
Как алюминий защищен от коррозии?
Канал ДНЕВНИК ПРОГРАММИСТА Жизнь программиста и интересные обзоры всего. , чтобы не пропустить новые видео.
Сплавы других металлов подвержены появлению ржавчины. Она проявляется достаточно быстро.
Если создать для алюминия определенные условия, то он не будет разрушаться долгие годы. Для защиты алюминия от коррозии на нем образуется специальная пленка. Она ложится тонким слоем, который составляет от 5 до 10 миллиметров.
Состоит подобное покрытие из оксида алюминия.
Пленка является прочной и дает металлу дополнительную защиту от внешних негативных воздействий. Благодаря такому слою воздух и влага не попадают в структуру материала. Если целостность оксидного покрытия нарушается, то начинается процесс коррозии алюминия. Металл теряет свои свойства.
Причины появления коррозии
Когда встает вопрос о том, ржавеет ли алюминий, необходимо задуматься о причинах, приводящих к коррозии. Различные внешние факторы могут ускорять этот процесс. Причины появления ржавчины на алюминии могут быть следующими:
Что такое электрохимическая коррозия и может ли она быть на листе алюминия?
Что такое «патриции»? Исторические сведения
Чаще всего появление электрохимической коррозии провоцируют гальванические пары. Повреждение появляется в месте соединения двух разных сплавов. В таком случае ржавчина будет явно бросаться в глаза.
Важным моментом является то, что портится только один металл, а второй является источником запуска коррозионного процесса. Чтобы не бояться электрохимической коррозии, нужно использовать магниевый сплав.
Специалисты из-за электрохимической ржавчины не рекомендуют использовать обычное железо при контакте с кузовом из алюминия.
Какие факторы могут замедлить процесс?
Существует ряд факторов, которые замедляют процессы коррозии алюминия, а некоторые из них останавливают подобное явление. Выделяют следующие:
При каких условиях начинается разрушение алюминия на воздухе
Альтернативность — это наличие выбора возможностей
Некоторые интересуются, ржавеет ли алюминий на воздухе. Если будет разрушена оксидная пленка на верхнем слое металла, то может начаться процесс коррозии. В результате может проявиться ржавчина. Рост пленки, как правило, замедляется на свежем воздухе. Следует помнить, что оксид алюминия отличается хорошей сцепкой с поверхностью металла.
Если лист хранится на складе, то пленка будет от 0,01 до 0,02 мкм. Если металл соприкасается с сухим кислородом, то толщина оксидной пленки на поверхности будет от 0,02 до 0,04 мкм. Если алюминий подвергают термической обработке, то толщина пленки изменяется. Она будет равна 0,1 мкм.
Считается, что алюминий обладает достаточной стойкостью, чтобы использовать его на свежем воздухе. Например, его применяют в сельской местности, а также в удаленных промышленных зонах.
Как вода воздействует на описываемый металл?
Коррозия алюминия в воде может наступить от повреждения верхнего слоя и защитной пленки. Высокая температура жидкости способствует скорейшему разрушению металла.
Если алюминий поместить в пресную воду, то коррозионные процессы практически не будут наблюдаться. Если повысить температуру воды, то изменений можно не заметить.
Когда жидкость нагревается до температуры 80 градусов и выше, то металл начинает портиться.
Скорость коррозии алюминия увеличивается, если в воду попадает щелочь. Описываемый металл обладает повышенной чувствительностью к соли. Именно поэтому морская вода для него губительна.
Чтобы использовать этот металл в морской воде, необходимо в жидкость добавлять магний или кремний.
Если использовать лист алюминия, в составе которого есть медь, то коррозия сплава будет протекать гораздо быстрее, чем у чистого вещества.
Опасна ли для алюминия серная кислота?
Люди интересуются, ржавеет ли алюминий в серной кислоте. Подобная кислота является потенциально опасной для сплавов. Она обладает ярко выраженными окислительными свойствами. Они разрушают оксидную пленку и ускоряют коррозию металла.
Интересным моментом является то, что концентрированная холодная сера не влияет на алюминий. Если алюминий нагреть, тогда могут начаться процессы коррозии металла. В таком случае появляется соль, ее называют сульфатом алюминия. Она растворима в воде.
Стойкость алюминия в азотной кислоте
Описываемый металл отличается повышенной стойкостью при попадании в раствор азотной кислоты. Его часто синтезируют для того, чтобы получить концентрированную азотную кислоту.
Какие вещества не оказывают воздействия на алюминий?
Не стоит бояться коррозионных процессов, если алюминий соприкоснется с лимонной кислотой. Не изменят свойства его сплава также яблочная кислота и фруктовый сок. Масляная слабо влияет на сплавы, в состав которых входит алюминий.
Будет ли происходить коррозия металла при контакте со щелочью?
Не стоит допускать контакта алюминия с различными щелочами. Они легко разрушают защитную пленку на верхнем слое. Металл вступает в реакцию с водой, после чего начинает выделяться водород. Процесс коррозии происходит в данном случае быстро. Ртуть и медь также пагубно влияют за защитный слой алюминия.
Итак, мы выяснили, ржавеет ли алюминий. Как видите, не всегда он имеет хорошую коррозионную защиту.
Источник
Как защитить металл от повреждения
В работе используется несколько видов защитных средств, к которым относятся такие, как:
Использование специальных лакокрасочных покрытий
Как и в случае с борьбой с ржавением под открытым воздухом, очень важно не допустить контакта агрессивной среды с металлом. ЛКМ в таком случае подходят отлично.
Есть несколько типов материалов, которые можно свободно использовать в окрашивании.
К ним относятся такие, как:
- Краски на основе битумов.
- Составы с фенолформальдегидной основой.
- Этинолевые лакокрасочные материалы.
Хорошо показывают себя вещества с эпоксидной, каменноугольной основой. Главное требование, чтобы в них было как можно меньше растворителей.
Главное преимущество использования такого средства заключается в простоте нанесения.
Краска наносится на поверхность, защищенные места сразу становятся хорошо видимыми.
Для дополнительного усиления, ограждающего от агрессивной среды эффекта, можно также применять разные окиси, в том числе, ртути и меди. В таком случае конструкция не будет обрастать морскими обитателями.
Чтобы нанесение ЛКМ дало лучшие результаты, поверхность металлоконструкции нужно будет фосфатировать. Только после этого допускается проведение окрашивания.
Стоит также учитывать, что оно должно быть как можно более толстым, чтобы удержаться дольше и сохранить заметный эффект.
Гальванические пары
Относительное расположение двух металлов или сплавов в гальваническом ряду указывает только возможность гальванической коррозии, если различие их гальванических потенциалов является достаточно большим. Больше этот ряд ничего не говорит, и особенно ничего – о скорости или интенсивности гальванической коррозии. Она может быть нулевой или несущественной или даже незаметной. Ее интенсивность зависит от типов металлов, которые входят в контакт – гальванической пары.
Пара: алюминий – нелегированная сталь
В строительных конструкциях алюминиевые детали, которые открыты для воздействия климатических и погодных воздействий, могут соединяться винтами из обычной стали. Опыт показывает, что алюминий в контакте со стальными винтами подвергается только очень поверхностной коррозии. Возникающая ржавчина, которая не оказывает никакого влияния на алюминий, полностью пропитывает слой оксида алюминия и образует на поверхности пятна. Фактически, для алюминиевой конструкции в контакте с незащищенной сталью важнее будет ее влияние на внешний вид и декоративные качества, а не способность сопротивляться коррозии.
Это явление имеет следующее объяснение:
- на поверхностях контакта образуются пленки с продуктами коррозии – ржавчины на стали и оксида алюминия на алюминии, которые и замедляют электрохимические реакции.
Пара: алюминий – оцинкованная сталь
Судя по гальваническому ряду, цинк является более электроотрицательным, чем алюминий. Крепеж из оцинкованной стали может, поэтому, применяться для соединения и сборки конструкций из алюминиевых сплавов. Надо помнить, что когда цинковое покрытие станет слишком изношенным, чтобы защищать сталь и алюминий, наступает предыдущий сценарий контакта между алюминием и голой сталью [3] .
Пара: алюминий – нержавеющая сталь
Хотя и существует большая разность потенциалов между нержавеющей сталью и алюминиевыми сплавами – около 650 мВ, очень редко можно увидеть гальваническую коррозию на алюминии в контакте с нержавеющей сталью. Поэтому алюминиевые конструкции очень часто собираются с применением болтов и винтов из нержавеющей стали [3].
Пара: алюминий – медь
Контакт между алюминиевыми сплавами и медью, а также медными сплавами (бронза, латунь) приводит к совершенно незначительной гальванической коррозии алюминия под воздействием атмосферных условий. Тем не менее, рекомендуется обеспечивать электрическую изоляцию между этими двумя металлами, чтобы локализовать коррозию алюминия.
Необходимо отметить, что продуктом коррозии меди является, так называемая, патина. Эта патина – голубовато-зеленый налет на меди, который состоит в основном из карбоната меди. Эта патина химически воздействует на алюминий и может восстанавливаться с образованием малых частиц меди. Эти медные частицы, в свою очередь, могут вызывать локальную питтинговую коррозию алюминия [3].
Защита методом горячего цинкования
Наша компания предлагает горячую оцинковку различных видов конструкций, в том числе тех, которые постоянно находятся в контакте с морской водой.
Работаем с 2007 года и готовы быстро выполнить даже наиболее сложный и крупный заказ.
4 причины обратиться к нам:
- Действуют три цеха горячего цинкования. Наши производственные мощности – 120 тысяч тонн в год.
- Работаем с большинством видов деталей и конструкций. На предприятии установлена самая крупная ванна в ЦФО. Ее глубина составляет 3,43 метра.
- Гарантируем качество. Горячее цинкование проводится строго по ГОСТ 9.307-89.
- Используем передовое оборудование. Установлена европейская техника от KVK KOERNER и EKOMOR.
Готовы ответить на все интересующие заказчика вопросы и быстро приступить к работе. Звоните или оставляйте заявку на сайте.
Вернуться к статьям Поделиться статьей