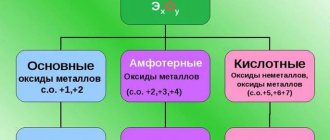
Аргон — благородный газ. Благородные газы — это 7 элементов в группе 18 (VIII A) периодической таблицы (Периодическая таблица представляет собой диаграмму, которая показывает, как химические элементы связаны друг с другом). Благородные газы также называют инертными газами, потому что элементы группы 18 (VIII A) реагируют с очень небольшим количеством других элементов. Фактически, никакого соединения аргона никогда не производилось.
Английский химик по имени Джон Уильям Струтт, наиболее известный как лорд Рэлей (1842-1919), химик Уильям Рамзи (1852-1916) открыл аргон в 1894 году. Это был первый выделенный вид благородных газов.
Рэлей и Рамзи нашли аргон фракционной перегонкой жидкого воздуха. Фракционная перегонка — это метод, позволяющий жидкому воздуху медленно нагреться. Когда воздух нагревается, различные элементы превращаются из жидкости обратно в газ. Часть воздуха, которая снова превращается в газ при -185,86 ° C (-302,55 ° F), представляет собой аргон.
Символ: Ar
Атомный номер: 18
Атомная масса: 39.948 а.
Семейство: Группа 18 (VIII A) Благородный газ
Произношение: AR-гон
Аргон используется для изготовления инертного одеяла для определенных промышленных операций. Инертная газовая оболочка предотвращает реакцию любых химических веществ в процессе работы с кислородом и другими небольшими веществами, присутствующими в воздухе. Аргон также используется при создании «неоновых» ламп и в лазерах.
История открытия
Предыстория открытия Ar началась в 1785 году. Выдающийся ученый и естествоиспытатель из Великобритании Генри Кэвендиш исследовал состав воздуха. Он подвергал азот окислению и взвешивал получившиеся окислы. По окончании опыта в сосуде оставался газ. Кэвендиш определил его объем в 0,8% от начального объема воздуха.
Состав этого газа ученый определить не смог. Спустя столетие к проблеме вернулись сэры Джон Рэлей и Уильям Рэмзи. В ходе проведенных опытов они обнаружили, что азот, выделенный из воздуха, имеет большую плотность, нежели азот, получаемый в ходе реакции разложения нитрита аммония.
в 1884 году им удалось выделить из воздуха некий газ, более плотный, чем азот. Это вещество имело одноатомную молекулярную структуру и было крайне инертным — т.е. не реагировало с другими веществами.
На заседании Королевского Общества новому газу было присвоено название «аргон», что в переводе с древнегреческого значило «спокойный, ленивый»
Аргон в природе
Ввиду практически полной инертности Ar представлен в естественной среде исключительно в несвязанном виде. Его процентная доля в различных частях Земли равна приблизительно:
- земная кора — 0,00012%;
- морская вода — 0,00045%;
- атмосфера — 0,926%.
Доля Ar в воздухе выше, чем суммарная доля всех остальных инертных газов. Основным источником для его добычи служит наша атмосфера.
Содержание газов в атмосфере
В коре Земли аргон содержится также в виде радиоактивного изотопа Аргон-40 и появляется в ходе реакции распада изотопов Калия.
Современная наука вместе с остальными инертными газообразными элементами относит Ar к VIII группе периодической системы.
Аргон
АРГОН относится к инертным, или благородным, газам. Простое вещество аргон — газ без запаха, цвета и вкуса.
Название: от греческого «argos» (недеятельный).
Физические свойства:
Аргон — одноатомный газ с температурой кипения (при нормальном давлении) –185,9°C (немного ниже, чем у кислорода, но немного выше, чем у азота), температура плавления –189,3°C. Критическая температура –122,43°C, критическое давление 4,86 МПа. Плотность при нормальных условиях 1,7839 кг/м3.
В 100 мл воды при 20°C растворяется 3,3 мл аргона, в некоторых органических растворителях аргон растворяется значительно лучше, чем в воде.
Получение:
В промышленности аргон получают как побочный продукт при крупномасштабном разделении воздуха на кислород и азот.
Обычно используют воздухоразделительные аппараты двукратной ректификации, состоящие из нижней колонны высокого давления (предварительное разделение), верхней колонны низкого давления и промежуточного конденсатора-испарителя. В конечном счете азот отводится сверху, а кислород – из пространства над конденсатором.
Летучесть аргона больше, чем кислорода, но меньше, чем азота. Поэтому аргонную фракцию отбирают в точке, находящейся примерно на трети высоты верхней колонны, и отводят в специальную колонну. Дальше следует очистка «сырого» аргона от кислорода (химическим путем или адсорбцией) и от азота (ректификацией).
Нахождение в природе:
Аргон распространен в природе только в свободном виде. В земной коре его содержание составляет 1,2·10–4 %, в морской воде — 0,45·10–4 %. В атмосферном воздухе содержится 0,93% аргона по объему (9,34 л в 1м3). Это значительно больше, чем содержание в воздухе всех остальных инертных газов вместе взятых. Воздух служит неиссякаемым источником для получения аргона.
Применение:
Аргон находит широкое применение благодаря своему основному свойству — химической неактивности.
Аргон широко используют для создания инертной и защитной атмосферы, прежде всего при термической обработке легко окисляющихся металлов (аргоновая плавка, аргоновая сварка и другие).
В атмосфере аргона получают кристаллы полупроводников и многие другие сверхчистые материалы.
Аргоном часто заполняют электрические лампочки (для замедления испарения вольфрама (W) со спирали). При пропускании электрического разряда через стеклянную трубку, заполненную аргоном, наблюдается сине-голубое свечение, что широко используется, например, в светящейся рекламе. Аргон используется для подсветки рекламных плакатов, стендов. Так называемые неоновые осветительные приборы на самом деле заполняются аргоном.
Однако в последние десятилетия наибольшая часть получаемого аргона идет не в лампочки, а в металлургию.
Уже существуют металлургические цеха объемом в несколько тысяч кубометров с атмосферой, состоящей из аргона высокой чистоты. В этих цехах работают в изолирующих костюмах, а дышат подаваемым через шланги воздухом (выдыхаемый воздух отводится также через шланги); запасные дыхательные аппараты закреплены на спинах работающих.
В среде аргона ведут процессы, при которых нужно исключить контакт расплавленного металла с кислородом, азотом, углекислотой и влагой воздуха. Аргонная среда используется при горячей обработке титана, тантала, ниобия, бериллия, циркония, гафния, вольфрама, урана, тория, а также щелочных металлов. В атмосфере аргона обрабатывают плутоний, получают некоторые соединения хрома, титана, ванадия и других элементов.
Продувкой аргона через жидкую сталь из нее удаляют газовые включения. Это улучшает свойства металла.
Все шире применяется дуговая электросварка в среде аргона. В аргонной струе можно сваривать тонкостенные изделия и металлы, которые прежде считались трудносвариваемыми. При сварке в аргонной струе нет надобности во флюсах и электродных покрытиях, а стало быть, и в зачистке шва от шлака и остатков флюса.
Аргон относится к инертным газам, которые химически не взаимодействуют с металлом и не растворяются в нем. Инертные газы применяют для сварки химически активных металлов (титан, алюминий, магний и др.), а также во всех случаях, когда необходимо получать сварные швы, однородные по составу с основным и присадочным металлом (высоколегированные стали и др.).
Инертные газы обеспечивают защиту дуги и свариваемого металла, не оказывая на него металлургического воздействия.
Аргон используется в плазменной сварке и резке металлов как плазмообразующий газ. При микроплазменной сварке большинство металлов сваривают в непрерывном или импульсном режимах дугой прямой полярности, горящей между вольфрамовым электродом плазмотрона и изделием в струе плазмообразующего инертного газа – (чаще всего) аргона.
Электрическая дуга в аргонной атмосфере внесла переворот в технику резки металлов. Процесс намного ускорился, появилась возможность резать толстые листы самых тугоплавких металлов. Продуваемый вдоль столба дуги аргон (в смеси с водородом) предохраняет кромки разреза и вольфрамовый электрод от образования окисных, нитридных и иных пленок. Одновременно он сжимает и концентрирует дугу на малой поверхности, отчего температура в зоне резки достигает 4000-6000°С. К тому же, эта газовая струя выдувает продукты резки.
Поскольку аргон обладает низкой теплопроводностью его используют при заполнении внутреннего пространства стеклопакетов.
Стремление использовать свойства и возможности сверхчистых материалов — одна из тенденций современной техники. Для сверхчистоты нужны инертные защитные среды, разумеется, тоже чистые; аргон — самый дешевый и доступный из благородных газов.
Аргон высокой чистоты применяют в спектроскопических установках для анализа чистоты материалов и в аргоновых лазерах.
В пищевой промышленности аргон зарегистрирован в качестве пищевой добавки E938, в качестве пропеллента и упаковочного газа.
Используется аргон и в качестве огнетушащего вещества в газовых установках пожаротушения.
Опасные факторы и меры безопасности
При всех своих преимуществах аргон достаточно опасен.
Может вызвать головокружение, тошноту, рвоту, потерю сознания и смерть от асфиксии (в результате кислородного голодания).
В жидком состоянии он способен вызвать обморожение кожи, слизистой оболочки при соприкосновении с ней, поэтому при работе с жидким аргоном необходимо соблюдать меры безопасности при обращении с жидкими криопродуктами.
Как добывают аргон
Благодаря значительному с промышленной точки зрения содержанию аргона в воздухе его получают в качестве дополнительного продукта криогенной ректификации O2 и N2.
Технология основана на том факте, что температура кипения (или сжижения) Ar лежит между температурами N2 и O2.
Перед началом процесса воздух подвергается тщательной очистке от пыли в многоступенчатых фильтрах, осушается от водяных паров, а далее мощными компрессорами сжимается до тех пор, пока не перейдет в жидкое состояние. Жидкость перегоняют в ректификационной колонне, чтобы разделить ее на отдельные вещества.
Установка для добычи аргона
Первым испаряется азот при -195 °С, его пары собираются на соответствующей тарелке ректификатора и отводятся в отдельный резервуар. Следующим по высоте (и при температуре кипения -185 °С) отбирается аргонная фракция, содержащая 12% Ar, менее полпроцента азота и кислород. Она подается в следующую ректификационную колонну, в которой процентная доля Ar доводится до 85, оставшееся приходится на кислород со следами азота. Такое вещество называется сырым аргоном, исходным материалом для получения очищенного газа.
В промышленности применяется несколько методов очистки сырого аргона от примесей.
Водород, добавляемый в состав сырья, окисляется на катализаторе и нагреве до 500 °С, таким образом, из состава смеси выводится кислород. Образовавшийся на катализаторе водяной пары удаляют при посредстве влагоотделителя. Газ после этого осушают. Аргон с оставшимся в нем азотом вновь ректифицируют.
Применяются и альтернативные методы получения Ar. Во время синтеза аммиака из азота и водорода в химических реакторах Ar получают как сопутствующий продукт производства. Технологический компонент это синтеза — продувочный газ — содержит до 20% Ar. Из этого газа и извлекают самый спокойный элемент. Стоимость производства, складывающаяся в основном из затрат на охлаждение и нагрев компонентов, делится между аммиаком и аргоном, и получается существенно ниже.
Качество газа, получаемого любым методом, определяется технологией очистки его от небольших количеств остаточного N2, O2, водяных паров и H2.
Аппарат, получающий ионные пучки аргона
Распространенность аргона
Аргон является одним из самых распространенных элементов во Вселенной. Частота его встречаемости сопоставима с частотой серы или алюминия. По распространенности во Вселенной среди благородных газов аргон занимает третье место после гелия и неона. Что же касается нашей планеты, то он занимает лидирующую позицию среди благородных газов. Его процентное содержание в атмосфере Земли составляет 0,934% от общего объема химических элементов по массе. Так же аргон занимает третью позицию после азота и кислорода в атмосфере Земли.
Стоит отметить то, что аргон образуется в результате распада калия. Поэтому его достаточно часто можно встретить в составе минералов и горных пород земной коры. Когда минералы в мантии начинают расплавляться аргон и гелий переходят в газообразное состояние. Эти свойства позволяют ему накапливаться в базальтах океанической воды. Так же его можно встретить в грунтовых и родниковых водах. Чем глубже источник родниковой воды, тем большее содержание аргона в его составе.
Читайте: Фосфор как химический элемент таблицы Менделеева
Общая характеристика Ar
Ar входит в группу инертных газов. Заряд его ядра — 18, под таким же номером элемент располагается в таблице Менделеева.
Из всех участников VIIIA группы он является наиболее часто встречающимся в природе. Объемная доля Ar в атмосфере -0,93%, массовая доля составляет 1,28%.Элемент является газом без цвета, вкуса и запаха. Химически не активен – аргон не вступает в реакцию и практически не соединяется ни с какими элементами или веществами, за исключением CU(Ar)O, и гидрофторида аргона.
Весьма плохо растворим водой, чуть большая растворимость наблюдается при взаимодействии с органическими растворителям.
Свойства аргона (таблица): температура, плотность, давление и пр.
Подробные сведения на сайте ChemicalStudy.ru
| 100 | Общие сведения | |
| 101 | Название | Аргон |
| 102 | Прежнее название | |
| 103 | Латинское название | Argon |
| 104 | Английское название | Argon |
| 105 | Символ | Ar |
| 106 | Атомный номер (номер в таблице) | 18 |
| 107 | Тип | Неметалл |
| 108 | Группа | Инертный (благородный) газ |
| 109 | Открыт | Уильям Рамзай, Джон Уильям Стретт (лорд Рэлей), Великобритания, 1894 г. |
| 110 | Год открытия | 1894 г. |
| 111 | Внешний вид и пр. | Инертный газ без цвета, вкуса и запаха |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | |
| 115 | Температура и иные условия перехода аллотропных модификаций друг в друга | |
| 116 | Конденсат Бозе-Эйнштейна | |
| 117 | Двумерные материалы | |
| 118 | Содержание в атмосфере и воздухе (по массе) | 1,292 % |
| 119 | Содержание в земной коре (по массе) | 0,00015 % |
| 120 | Содержание в морях и океанах (по массе) | 0,000045 % |
| 121 | Содержание во Вселенной и космосе (по массе) | 0,02 % |
| 122 | Содержание в Солнце (по массе) | 0,007 % |
| 123 | Содержание в метеоритах (по массе) | |
| 124 | Содержание в организме человека (по массе) | |
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса) | 39,948(1) а. е. м. (г/моль) |
| 202 | Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 |
| 203 | Электронная оболочка | K2 L8 M8 N0 O0 P0 Q0 R0 |
| 204 | Радиус атома (вычисленный) | 71 пм |
| 205 | Эмпирический радиус атома | |
| 206 | Ковалентный радиус* | 106 пм |
| 207 | Радиус иона (кристаллический) | |
| 208 | Радиус Ван-дер-Ваальса | 188 пм |
| 209 | Электроны, Протоны, Нейтроны | 18 электронов, 18 протонов, 22 нейтронов |
| 210 | Семейство (блок) | элемент p-семейства |
| 211 | Период в периодической таблице | 3 |
| 212 | Группа в периодической таблице | 18-ая группа (по старой классификации – главная подгруппа 8-ой группы) |
| 213 | Эмиссионный спектр излучения | |
| 300 | Химические свойства | |
| 301 | Степени окисления | 0 |
| 302 | Валентность | 0 |
| 303 | Электроотрицательность | 4,3 (шкала Полинга) |
| 304 | Энергия ионизации (первый электрон) | 1520,57 кДж/моль (15,7596117(5) эВ) |
| 305 | Электродный потенциал | 0 |
| 306 | Энергия сродства атома к электрону | -96(20) кДж/моль (-1,0(2) эВ) – предположительно |
| 400 | Физические свойства | |
| 401 | Плотность* | 0,001784 г/см3 (при 0 °C и иных стандартных условиях, состояние вещества – газ), 1,3954 г/см3 (при температуре кипения -185,848 °C и иных стандартных условиях, состояние вещества – жидкость), 1,65 г/см3 (при -233 °C и иных стандартных условиях, состояние вещества – твердое тело) |
| 402 | Температура плавления* | -189,34 °C (83,81 K, -308,81 °F) |
| 403 | Температура кипения* | -185,848 °C (87,302 K, -302,526 °F) |
| 404 | Температура сублимации | |
| 405 | Температура разложения | |
| 406 | Температура самовоспламенения смеси газа с воздухом | |
| 407 | Удельная теплота плавления (энтальпия плавления ΔHпл)* | 1,18 кДж/моль |
| 408 | Удельная теплота испарения (энтальпия кипения ΔHкип)* | 6,53 кДж/моль |
| 409 | Удельная теплоемкость при постоянном давлении | |
| 410 | Молярная теплоёмкость* | 20,85 Дж/(K·моль) |
| 411 | Молярный объём | 22,392 см³/моль |
| 412 | Теплопроводность | 17,72·10-3 Вт/(м·К) (при стандартных условиях), 0,0164 Вт/(м·К) (при 300 K) |
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | |
| 512 | Структура решётки | Кубическая гранецентрированная |
| 513 | Параметры решётки | 5,260 Å |
| 514 | Отношение c/a | |
| 515 | Температура Дебая | 85 К |
| 516 | Название пространственной группы симметрии | Fm_ 3m |
| 517 | Номер пространственной группы симметрии | 225 |
| 900 | Дополнительные сведения | |
| 901 | Номер CAS | 7440-37-1 |
Примечание:
206* Ковалентный радиус аргона согласно [1] составляет 106±10 пм.
401* Плотность аргона согласно [3] и [4] [Россия] составляет 0,0017839 г/см3 (при 0 °C /20 °C и иных стандартных условиях, состояние вещества – газ).
402* Температура плавления аргона согласно [3] и [4] составляет -189,35 °C (83,8 K, -308,83 °F) и -189,6 °C (83,55 K, -309,28 °F) соответственно.
403* Температура кипения аргона согласно [3] и [4] составляет -185,85 °C (87,3 K, -302,53 °F) и -185,9 °C (87,25 K, -302,62 °F) соответственно.
407* Удельная теплота плавления (энтальпия плавления ΔHпл) аргона согласно [3] и [4] составляет 7,05 кДж/моль и 1,19 кДж/моль соответственно.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) аргона согласно [3] и [4] составляет 6,45 кДж/моль и 6,51 кДж/моль соответственно.
410* Молярная теплоемкость аргона [3] составляет 20,79 Дж/(K·моль).
Виды аргона
Говоря о видах, или сортах Ar, надо понимать, что это одно и то же химическое вещество. Виды различаются по степени очистки от примесей.
- Высший сорт. Содержание Ar не менее 99,99% . Этот сорт особо высокой чистоты применяется для ответственных сварочных работ, таких, как сварка материалов, химически активных в нагретом состоянии: некоторые цветные сплавы, прежде всего титановые, нержавеющая сталь и др. Используется также для сварки высоконагруженных изделий из конструкционной стали.
- Первый сорт. Содержание Ar не менее 99,98%, Применяется при сварке сплавов на основе алюминия с другими металлами и сплавами, для менее активных цветных металлов.
- Второй сорт. Содержание Ar не менее 99,95%. Используется при сваривании деталей из жаростойких стальных сплавов, алюминия и конструкционных сталей. Применение чистого Ar в этих случаях нежелательно, поскольку приводит к повышенной пористости материала шва и не позволяет защитить сварочную ванну от повышенной влажности и других загрязнений. Во избежание возникновения такого дефекта в состав смеси защитных газов добавляют углекислый газ и кислород, связывающие выделяющийся при сварке водород и другие примеси. Образующиеся в ходе этих реакций шлаки всплывают на поверхность сварочной ванны и после застывания удаляются вместе с окалиной.
Химические свойства Аргон Argon
Определение химических свойств Argon —
Пока известны только 2 химических соединения аргона — гидрофторид аргона и CU(Ar)O, которые существуют при очень низких температурах. Кроме того, аргон образует эксимерные молекулы, то есть молекулы, у которых устойчивы возбуждённые электронные состояния и неустойчиво основное состояние. Есть основания считать, что исключительно нестойкое соединение Hg—Ar, образующееся в электрическом разряде, — это подлинно химическое (валентное) соединение. Не исключено, что будут получены другие валентные соединения аргона с фтором и кислородом, которые тоже должны быть крайне неустойчивыми. Например, при электрическом возбуждении смеси аргона и хлора возможна газофазная реакция с образованием ArCl. Также со многими веществами, между молекулами которых действуют водородные связи (водой, фенолом, гидрохиноном и другими), образует соединения включения (клатраты), где атом аргона, как своего рода «гость», находится в полости, образованной в кристаллической решётке молекулами вещества-хозяина, например, Ar·6H2O.
Соединение CU(Ar)O получено из соединения урана с углеродом и кислородом CUO[9]. Вероятно существование соединений со связями Ar-Si и Ar-C: FArSiF3 и FArCCH.
Физические и химические свойства
Свойства аргона типичны для члена VIII группы.
При обычной температуре Ar пребывает в газообразном состоянии. Молекула включает в себя единственный атома, химическая формула весьма простая: Ar. Температура кипения весьма низка : -185,8 °С при атмосферном уровне давления.
Растворимость в воде низкая — всего 3,29 мл на 100 мл жидкости
Плотность аргона при нормальных условиях составляет 1,78 кг/м3. Молярная теплоемкость газа- 20,7 Дж/Кмоль.
Характеристики аргона и других инертных газов
Газ практически полностью инертен. На сегодняшний день ученым удалось получить лишь два его соединения — CU(Ar)O, и гидрофторид аргона. Соединения существуют лишь при сверхнизких температурах. Предполагается, что Ar может входить в состав неустойчивых в нормальном состоянии молекул эксимерного типа. Такие молекулы могут существовать лишь в возбужденном состоянии, например, в ходе электроразряда высокой интенсивности. Такие соединения возможны с ртутью, кислородом и фтором.
Электроотрицательность по шкале Полинга равна 4,3.
Как степень окисления, так и электродный потенциал имеют нулевое значение, что характерно для инертного газа.
Ионный радиус составляет 154, радиус ковалентности — 106 Пм. Ионизационный порог- 1519 кдж/моль
Атомная и молекулярная масса
Такие важные параметры, как атомная и молекулярная массы, показывают, насколько масса молекулы вещества и масса его атома соответственно превышают значение, равное одной двенадцатой доле массы атома водорода.
Ввиду того, что молекула Ar состоит из единственного атома, молекулярная и атомная масса аргона идентичны и составляют 39,984.
Структура аргона и его свойства
Изотопы
В природных условиях Ar встречается в качестве трех устойчивых изотопов
- 36Ar– процентная доля этого изотопа составляет 0,337% в ядре 18 протонов и 18 нейтронов;
- 38Ar- его доля всего 0,063%, в ядре 18 протонов и 20 нейтронов;
- 40Ar – наиболее распространен, его доля составляет 99,6%, в ядре так же 18 протонов, но уже 22 нейтрона.
Искусственным путем удавалось получать изотопы с массовым индексом от 32 до 55, наиболее стабильным из них оказался 39Ar, период полураспада которого составляет 268 лет.
Большая процентная доля 40Ar среди изотопов, встречающихся в природе, вызвана постоянным образованием его в ходе реакции распада изотопа калий-40. На 1000 кг калия в ходе таких реакций за год образуется не более 3100 атомов 40Ar. Но, поскольку эти реакции идут постоянно в течение сотен миллионов лет, изотоп накопился в природе в существенных объемах.
Доминирование тяжелого изотопа в природе обуславливает тот факт, что атомный вес Ar превышает атомный вес калия, находящегося в таблице следом за ним. При создании Периодической системы такого противоречия не было, поскольку аргон был обнаружен и свойства его были исследованы значительно позже, в первом десятилетии XX века. Первоначально Ar был помещен в первую группу таблицы, восьмая группа была выделена позднее.
Ионы
Как и другие инертные газы (такие, как He и Ne), Ar подвержен ионизации. При возбуждении атомов и сообщении им высоких энергий возникают молекулярные ионы Ar2+.
Молекула и атом
Для инертных газов эти понятия идентичны, поскольку эти элементы не желают вступать в химическую связь даже с себе подобными. Молекула включает в себя один атом, химическая формула газа не отличается от обозначения элемента: Ar.
Молярная масса
Молярная масса аргона составляет 39,95 г/моль.
Существуют несколько методов ее вычисления:
- С применением относительной атомной массы M и коэффициента пропорциональности к, выражающего соотношение между относительной массой и молярной. Этот коэффициент является универсальной константой и равен для всех элементов. Молярная масса M выражается как произведение коэффициента пропорциональности на относительную массу.
- С использованием молярного объема. Потребуется найти объем, занимаемый при обычных условиях некоторой массой газа, далее рассчитать массу 22,4 литров вещества при таких же условиях.
- С применением уравнения Менделеева-Клапейрона, моделирующего идеальный газ.
pV = mRT / M,
проведя преобразования, получим выражение для молярной массы:
M=mRT/pV
где
- p – давление в паскалях,
- V –объем в кубометрах
- m – масса в граммах,
- Т — температура в Кельвинах,
- R – константа, значение которой 8,314 Дж/(моль×К).
Свойства атома аргона:
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса) | 39,948(1) а.е.м. (г/моль) |
| 202 | Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 |
| 203 | Электронная оболочка | K2 L8 M8 N0 O0 P0 Q0 R0 |
| 204 | Радиус атома (вычисленный) | 71 пм |
| 205 | Эмпирический радиус атома | |
| 206 | Ковалентный радиус* | 106 пм |
| 207 | Радиус иона | 154 пм |
| 208 | Радиус Ван-дер-Ваальса | 188 пм |
| 209 | Электроны, Протоны, Нейтроны | 18 электронов, 18 протонов, 22 нейтронов |
| 210 | Семейство (блок) | элемент p-семейства |
| 211 | Период в периодической таблице | 3 |
| 212 | Группа в периодической таблице | 18-ая группа (по старой классификации – главная подгруппа 8-ой группы) |
| 213 | Эмиссионный спектр излучения |
Область применения
Шире всего аргон применяется при сварочных работах. Он используется для создания защитной атмосферы вокруг сварочной ванны, вытесняя из рабочей зоны O2 и N2, содержащиеся в атмосфере. Особенно важно это для сварки цветных металлов, многие из которых, к примеру, Ti, отличаются высокой химической активностью в нагретом состоянии. Незаменим инертный газ также для неразъемного соединения нержавеющих и высоколегированных сплавов.
Также широко применяется при монтаже высоконагруженных строительных конструкций, таких, как каркасы высотных зданий, фермы мостов и многих других. Здесь его применение обеспечивает высокое качество, однородность и долговечность ответственных соединений. В строительной индустрии аргонная сварка доминирует среди других методов.
Сварка аргоном
Аргонно-дуговая сварка
Не менее широко применяется аргонная сварка в машиностроении, прежде всего химическом и пищевом. Швы получаются долговечные и надежные, даже в условиях воздействия агрессивных сред.
Нефтяная и газовая отрасли также применяют аргонная сварку при монтаже трубопроводов, газоперекачивающих станций и нефтеперегонных комбинатов.
Используется метод также в атомной промышленности, в транспортном машиностроении и в аэрокосмической отрасли.
В домохозяйствах аргонная сварка распространена не так широко. Это объясняется:
- высокой стоимостью оборудования и расходных материалов;
- необходимостью достаточной квалификации сварщика;
- меньшими нагрузками, испытываемыми домашними конструкциями;
- более низкими требованиями к прочности и долговечности сварных соединений.
Если в домохозяйстве возникает эпизодическая потребность в таких сварочных работах, то дешевле, быстрее и надежнее пригласить сварщика-специалиста.
Стеклопакет с аргоном
Принцип действия стеклопакета с аргоном
Характерным свойством Ar является его более высокая плотность по сравнению с воздухом. Поэтому максимальная эффективность аргонной сварки достигается при нижнем сварочном положении. В этом случае инертный раз растекается по поверхности детали и образует защитное облако значительной протяженности, позволяя вести сварку, как большими токами, так и на большой скорости. При сварке в наклонном и верхнем положении приходится учитывать «проваливание» аргона сквозь воздух. Чтобы компенсировать это явление, либо увеличивают подачу газа, либо проводят работы в герметичном помещении, заполненным инертным газом. В обоих случаях себестоимость работ возрастает.
Поскольку потенциал ионизации Ar невысок, его использование обеспечивает идеальные геометрических характеристик сварочного шва, прежде всего, профиля. Возбужденная электродуга в аргоновой атмосфере также отличается высокой стабильностью своих параметров. С другой стороны, низкое значение потенциала ионизации обуславливает и более низкое напряжение розжига и поддержания дуги. Это сокращает ее тепловыделение и усложняет провар толстых листов металла.
Более высокая температура дуги в аргоновой атмосфере существенно повышает проплав сварочного шва. Это позволяет проводить сварку за один проход при условии точного соблюдения параметров зазора между заготовками.
В случае применения TIG-метода сварочных работ аргоновая атмосфера защищает от коррозионного влияния не только зону сварки, но и окончание неплавкого электрода.
В ряде специфических случаев в состав защитной газовой смеси добавляют гелий.
Кроме применения при сварочных работах, аргон используется:
- Как плазмоообразующее веществона установках плазменного раскроя металла.
- Для создания инертной среды в упаковках пищевых продуктов. Он вытесняет из пакетов и контейнеров кислород воздуха и водяные пары, пагубно влияющие на срок годности продуктов. Продукты в защитной атмосфере хранятся в несколько раз дольше, чем в обычной упаковке. Применяется этот метод и для упаковки медицинских изделий и препаратов, позволяя сохранить их в должной стерильности и химической чистоте.
- В качестве активного агента в противопожарных установках. Аргон вытесняет кислород (или другой газ) из очага горения, прекращая его.
- Для создания защитной среды в технологических установках при обработке полупроводниковых устройств, создании микросхем и других электронных компонентов или материалов высоких степеней чистоты.
- Наполнитель электроламп.
- В рекламных люминесцентных трубках.
Применение
Ниже перечислены области применения аргона:
- в аргоновых лазерах;
- в лампах накаливания и при заполнении внутреннего пространства стеклопакетов;
- в качестве защитной среды при сварке (дуговой, лазерной, контактной и т. п.) как металлов (например, титана), так и неметаллов;
- в качестве плазмаобразователя в плазматронах при сварке и резке;
- в пищевой промышленности аргон зарегистрирован в качестве пищевой добавки E938
, в качестве пропеллента и упаковочного газа; - в качестве огнетушащего вещества в газовых установках пожаротушения;
- в медицине во время операций для очистки воздуха и разрезов, так как аргон не образует химических соединений при комнатной температуре;
- в качестве составной части атмосферы эксперимента «Марс-500»[10] с целью снижения уровня кислорода для предотвращения пожара на борту космического корабля при путешествии на Марс;
- из-за низкой теплопроводности аргон применяется в дайвинге для поддува сухих гидрокостюмов, однако есть ряд недостатков, например, высокая цена газа (кроме этого, нужна отдельная система для аргона);
- в химическом синтезе для создания инертной атмосферы при работе с нестабильными на воздухе соединениями.
Зависимость давления аргона в баллоне от температуры
По мере нагрева давление газообразного вещества в замкнутом объеме повышается. В таблице приведены примерные значения давления в баллоне в зависимости от температуры окружающего воздуха.
| T, °C | P, Мегапаскаль |
| -40 | 10,45 |
| -30 | 11,33 |
| -20 | 12,21 |
| -10 | 12,92 |
| 0 | 13,74 |
| +10 | 14,62 |
| +20 | 15,33 |
| +30 | 16,03 |
Следует учитывать, что баллонное давление изменяется не мгновенно, а по мере его прогрева или охлаждения.